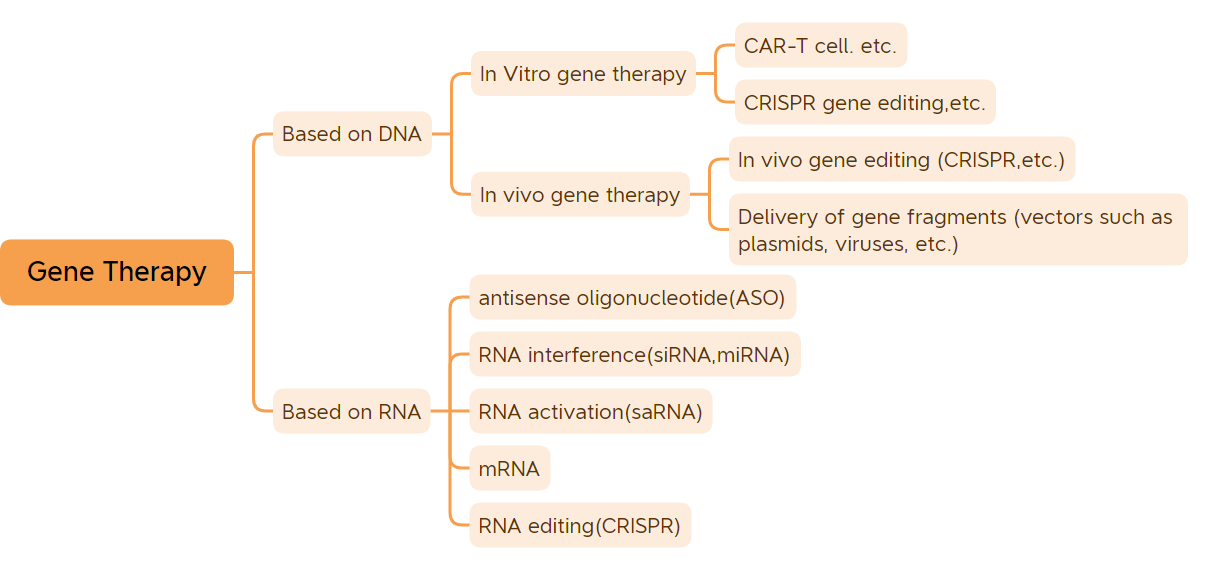
ಜೀನ್ಗಳು ಗುಣಲಕ್ಷಣಗಳನ್ನು ನಿಯಂತ್ರಿಸುವ ಮೂಲ ಆನುವಂಶಿಕ ಘಟಕಗಳಾಗಿವೆ.ಆರ್ಎನ್ಎಯಿಂದ ರಚಿತವಾಗಿರುವ ಕೆಲವು ವೈರಸ್ಗಳ ಜೀನ್ಗಳನ್ನು ಹೊರತುಪಡಿಸಿ, ಹೆಚ್ಚಿನ ಜೀವಿಗಳ ಜೀನ್ಗಳು ಡಿಎನ್ಎಯಿಂದ ಕೂಡಿದೆ.ಜೀವಿಗಳ ಹೆಚ್ಚಿನ ರೋಗಗಳು ಜೀನ್ಗಳು ಮತ್ತು ಪರಿಸರದ ನಡುವಿನ ಪರಸ್ಪರ ಕ್ರಿಯೆಯಿಂದ ಉಂಟಾಗುತ್ತವೆ.ಜೀನ್ ಚಿಕಿತ್ಸೆಯು ಮೂಲಭೂತವಾಗಿ ಅನೇಕ ರೋಗಗಳನ್ನು ಗುಣಪಡಿಸಬಹುದು ಅಥವಾ ನಿವಾರಿಸಬಹುದು.ವಂಶವಾಹಿ ಚಿಕಿತ್ಸೆಯು ಔಷಧ ಮತ್ತು ಔಷಧಾಲಯ ಕ್ಷೇತ್ರದಲ್ಲಿ ಒಂದು ಕ್ರಾಂತಿ ಎಂದು ಪರಿಗಣಿಸಲಾಗಿದೆ.ವ್ಯಾಪಕ ಅರ್ಥದಲ್ಲಿ ಜೀನ್ ಥೆರಪಿ ಔಷಧಗಳು ಡಿಎನ್ಎ-ಮಾರ್ಪಡಿಸಿದ ಡಿಎನ್ಎ ಔಷಧಗಳ ಆಧಾರದ ಮೇಲೆ ಸೇರಿವೆ (ವೈರಲ್ ವೆಕ್ಟರ್ಗಳನ್ನು ಆಧರಿಸಿದ ವಿವೋ ಜೀನ್ ಥೆರಪಿ ಡ್ರಗ್ಗಳು, ಇನ್ ವಿಟ್ರೊ ಜೀನ್ ಥೆರಪಿ ಡ್ರಗ್ಸ್, ನೇಕೆಡ್ ಪ್ಲಾಸ್ಮಿಡ್ ಡ್ರಗ್ಸ್, ಇತ್ಯಾದಿ.) ಮತ್ತು ಆರ್ಎನ್ಎ ಔಷಧಗಳು (ಆಂಟಿಸೆನ್ಸ್ ಆಲಿಗೊನ್ಯೂಕ್ಲಿಯೊಟೈಡ್ ಔಷಧಗಳು, ಸಿಆರ್ಎನ್ಎ ಔಷಧಗಳು ಮತ್ತು ಎಂಆರ್ಎನ್ಎ ಜೀನ್ ಥೆರಪಿ ಇತ್ಯಾದಿ);ಸಂಕುಚಿತ ಅರ್ಥದಲ್ಲಿ ಜೀನ್ ಥೆರಪಿ ಔಷಧಗಳು ಮುಖ್ಯವಾಗಿ ಪ್ಲಾಸ್ಮಿಡ್ ಡಿಎನ್ಎ ಔಷಧಗಳು, ವೈರಲ್ ವಾಹಕಗಳ ಆಧಾರದ ಮೇಲೆ ಜೀನ್ ಥೆರಪಿ ಔಷಧಗಳು, ಬ್ಯಾಕ್ಟೀರಿಯಾದ ವಾಹಕಗಳ ಆಧಾರದ ಮೇಲೆ ಜೀನ್ ಥೆರಪಿ ಔಷಧಗಳು, ಜೀನ್ ಎಡಿಟಿಂಗ್ ಸಿಸ್ಟಮ್ಗಳು ಮತ್ತು ವಿಟ್ರೊ ಜೀನ್ ಮಾರ್ಪಾಡಿಗಾಗಿ ಸೆಲ್ ಥೆರಪಿ ಔಷಧಗಳನ್ನು ಒಳಗೊಂಡಿರುತ್ತದೆ.ವರ್ಷಗಳ ನಂತರದ ಬೆಳವಣಿಗೆಯ ನಂತರ, ಜೀನ್ ಥೆರಪಿ ಔಷಧಿಗಳು ಉತ್ತೇಜಕ ಕ್ಲಿನಿಕಲ್ ಫಲಿತಾಂಶಗಳನ್ನು ಸಾಧಿಸಿವೆ.(ಡಿಎನ್ಎ ಲಸಿಕೆಗಳು ಮತ್ತು ಎಮ್ಆರ್ಎನ್ಎ ಲಸಿಕೆಗಳನ್ನು ಲೆಕ್ಕಿಸುವುದಿಲ್ಲ) ಪ್ರಸ್ತುತ, 45 ಜೀನ್ ಥೆರಪಿ ಔಷಧಿಗಳನ್ನು ಪ್ರಪಂಚದಲ್ಲಿ ಮಾರುಕಟ್ಟೆಗೆ ಅನುಮೋದಿಸಲಾಗಿದೆ.ಈ ವರ್ಷ ಮಾರ್ಕೆಟಿಂಗ್ಗಾಗಿ ಒಟ್ಟು 9 ವಂಶವಾಹಿ ಚಿಕಿತ್ಸೆಗಳನ್ನು ಅನುಮೋದಿಸಲಾಗಿದೆ, ಈ ವರ್ಷ ಮೊದಲ ಬಾರಿಗೆ ಮಾರ್ಕೆಟಿಂಗ್ಗೆ ಅನುಮೋದಿಸಲಾದ 7 ಜೀನ್ ಚಿಕಿತ್ಸೆಗಳು ಸೇರಿದಂತೆ, ಅವುಗಳೆಂದರೆ: ಕಾರ್ವೈಕ್ಟಿ, ಅಂವುತ್ರಾ, ಅಪ್ಸ್ಟಾಜಾ, ರೋಕ್ಟೇವಿಯನ್, ಹೆಮ್ಜೆನಿಕ್ಸ್, ಅಡ್ಸ್ಟಿಲಾಡ್ರಿನ್ ಮತ್ತು ಎಬ್ವಾಲ್ಲೋ, (ಗಮನಿಸಿ: ಈ ವರ್ಷದ ಮೊದಲ ಜೀನ್ ಥೆರಪಿಯನ್ನು ಯುನೈಟೆಡ್ ಸ್ಟೇಟ್ಸ್ನಲ್ಲಿ ಅನುಮೋದಿಸಲಾಗಿದೆ. ಆಗಸ್ಟ್ 2022 ರಲ್ಲಿ ಯುನೈಟೆಡ್ ಸ್ಟೇಟ್ಸ್ನಲ್ಲಿ ಮಾರ್ಕೆಟಿಂಗ್ಗಾಗಿ ಎಫ್ಡಿಎ ಅನುಮೋದಿಸಿತು ಮತ್ತು 2019 ರಲ್ಲಿ ಯುರೋಪಿಯನ್ ಯೂನಿಯನ್ನಿಂದ ಮಾರ್ಕೆಟಿಂಗ್ಗೆ ಅನುಮೋದಿಸಲಾಗಿದೆ; .) ಹೆಚ್ಚು ಹೆಚ್ಚು ಜೀನ್ ಥೆರಪಿ ಉತ್ಪನ್ನಗಳ ಉಡಾವಣೆ ಮತ್ತು ಜೀನ್ ಥೆರಪಿ ತಂತ್ರಜ್ಞಾನದ ಕ್ಷಿಪ್ರ ಅಭಿವೃದ್ಧಿಯೊಂದಿಗೆ, ಜೀನ್ ಚಿಕಿತ್ಸೆಯು ಕ್ಷಿಪ್ರ ಅಭಿವೃದ್ಧಿಯ ಅವಧಿಯನ್ನು ಪ್ರಾರಂಭಿಸಲಿದೆ.
ಜೀನ್ ಚಿಕಿತ್ಸೆಯ ವರ್ಗೀಕರಣ (ಚಿತ್ರ ಮೂಲ: ಬಯೋ-ಮ್ಯಾಟ್ರಿಕ್ಸ್)
ಈ ಲೇಖನವು ಮಾರ್ಕೆಟಿಂಗ್ಗಾಗಿ ಅನುಮೋದಿಸಲಾದ 45 ವಂಶವಾಹಿ ಚಿಕಿತ್ಸೆಗಳನ್ನು (ಡಿಎನ್ಎ ಲಸಿಕೆಗಳು ಮತ್ತು ಎಮ್ಆರ್ಎನ್ಎ ಲಸಿಕೆಗಳನ್ನು ಹೊರತುಪಡಿಸಿ) ಪಟ್ಟಿಮಾಡುತ್ತದೆ.
1. ಇನ್ ವಿಟ್ರೊ ಜೀನ್ ಥೆರಪಿ
(1) ಸ್ಟ್ರಿಮ್ವೆಲಿಸ್
ಕಂಪನಿ: ಗ್ಲಾಕ್ಸೊ ಸ್ಮಿತ್ಕ್ಲೈನ್ (GSK) ಅಭಿವೃದ್ಧಿಪಡಿಸಿದೆ.
ಮಾರುಕಟ್ಟೆಗೆ ಸಮಯ: ಮೇ 2016 ರಲ್ಲಿ ಯುರೋಪಿಯನ್ ಯೂನಿಯನ್ನಿಂದ ಮಾರ್ಕೆಟಿಂಗ್ಗಾಗಿ ಇದನ್ನು ಅನುಮೋದಿಸಲಾಗಿದೆ.
ಸೂಚನೆಗಳು: ತೀವ್ರವಾದ ಸಂಯೋಜಿತ ಇಮ್ಯುನೊಡಿಫೀಶಿಯೆನ್ಸಿ (SCID) ಚಿಕಿತ್ಸೆಗಾಗಿ.
ಟೀಕೆಗಳು: ಈ ಚಿಕಿತ್ಸೆಯ ಸಾಮಾನ್ಯ ಪ್ರಕ್ರಿಯೆಯು ಮೊದಲು ರೋಗಿಯ ಸ್ವಂತ ಹೆಮಟೊಪಯಟಿಕ್ ಕಾಂಡಕೋಶಗಳನ್ನು ಪಡೆಯುವುದು, ಅವುಗಳನ್ನು ವಿಟ್ರೊದಲ್ಲಿ ವಿಸ್ತರಿಸುವುದು ಮತ್ತು ಬೆಳೆಸುವುದು, ನಂತರ ರೆಟ್ರೊವೈರಸ್ ಅನ್ನು ಬಳಸಿಕೊಂಡು ಕ್ರಿಯಾತ್ಮಕ ADA (ಅಡೆನೊಸಿನ್ ಡೀಮಿನೇಸ್) ಜೀನ್ ಪ್ರತಿಯನ್ನು ಹೆಮಟೊಪಯಟಿಕ್ ಕಾಂಡಕೋಶಗಳಿಗೆ ಪರಿಚಯಿಸುವುದು ಮತ್ತು ಅಂತಿಮವಾಗಿ ಮಾರ್ಪಡಿಸಿದ ಹೆಮಟೊಪಯಟಿಕ್ ಕಾಂಡಕೋಶಗಳಿಗೆ ಮರುಕಳಿಸುವ ದೇಹಕ್ಕೆ ಚುಚ್ಚುವುದು.ಸ್ಟ್ರಿಮ್ವೆಲಿಸ್ನೊಂದಿಗೆ ಚಿಕಿತ್ಸೆ ಪಡೆದ ADA-SCID ರೋಗಿಗಳ 3-ವರ್ಷದ ಬದುಕುಳಿಯುವಿಕೆಯ ಪ್ರಮಾಣವು 100% ಎಂದು ಕ್ಲಿನಿಕಲ್ ಫಲಿತಾಂಶಗಳು ತೋರಿಸುತ್ತವೆ.
(2) ಝಲ್ಮೋಕ್ಸಿಸ್
ಕಂಪನಿ: ಇಟಲಿ MolMed ಕಂಪನಿಯಿಂದ ತಯಾರಿಸಲ್ಪಟ್ಟಿದೆ.
ಮಾರುಕಟ್ಟೆಗೆ ಸಮಯ: 2016 ರಲ್ಲಿ ಯುರೋಪಿಯನ್ ಒಕ್ಕೂಟದಿಂದ ಷರತ್ತುಬದ್ಧ ಮಾರ್ಕೆಟಿಂಗ್ ಅಧಿಕಾರವನ್ನು ಪಡೆದುಕೊಂಡಿದೆ.
ಸೂಚನೆಗಳು: ಹೆಮಟೊಪಯಟಿಕ್ ಕಾಂಡಕೋಶ ಕಸಿ ನಂತರ ರೋಗಿಗಳ ಪ್ರತಿರಕ್ಷಣಾ ವ್ಯವಸ್ಥೆಯ ಸಹಾಯಕ ಚಿಕಿತ್ಸೆಗಾಗಿ ಇದನ್ನು ಬಳಸಲಾಗುತ್ತದೆ.
ಟೀಕೆಗಳು: Zalmoxis ಎಂಬುದು ರೆಟ್ರೊವೈರಲ್ ವೆಕ್ಟರ್ಗಳಿಂದ ಮಾರ್ಪಡಿಸಲಾದ ಅಲೋಜೆನಿಕ್ ಟಿ ಸೆಲ್ ಸುಸೈಡ್ ಜೀನ್ ಇಮ್ಯುನೊಥೆರಪಿಯಾಗಿದೆ.ಈ ವಿಧಾನವು ಅಲೋಜೆನಿಕ್ ಟಿ ಕೋಶಗಳನ್ನು ತಳೀಯವಾಗಿ ಮಾರ್ಪಡಿಸಲು ರೆಟ್ರೊವೈರಲ್ ವೆಕ್ಟರ್ಗಳನ್ನು ಬಳಸುತ್ತದೆ, ಇದರಿಂದಾಗಿ ತಳೀಯವಾಗಿ ಮಾರ್ಪಡಿಸಿದ ಟಿ ಕೋಶಗಳು 1NGFR ಮತ್ತು HSV-TK Mut2 ಆತ್ಮಹತ್ಯಾ ಜೀನ್ಗಳನ್ನು ಜನರು ಯಾವುದೇ ಸಮಯದಲ್ಲಿ ಗ್ಯಾನ್ಸಿಕ್ಲೋವಿರ್ (ಗ್ಯಾನ್ಸಿಕ್ಲೋವಿರ್) ಔಷಧಗಳನ್ನು ಬಳಸಲು ಅನುಮತಿಸುತ್ತವೆ, ಇದು ಪ್ರತಿಕೂಲ ಪ್ರತಿರಕ್ಷಣಾ ಪ್ರತಿಕ್ರಿಯೆಗಳನ್ನು ಉಂಟುಮಾಡುತ್ತದೆ. .
(3) ಇನ್ವೊಸ್ಸಾ-ಕೆ
ಕಂಪನಿ: ಟಿಶ್ಯೂಜೀನ್ (ಕೊಲೊನ್ ಟಿಶ್ಯೂಜೆನ್) ಅಭಿವೃದ್ಧಿಪಡಿಸಿದೆ.
ಮಾರುಕಟ್ಟೆಗೆ ಸಮಯ: ಜುಲೈ 2017 ರಲ್ಲಿ ದಕ್ಷಿಣ ಕೊರಿಯಾದಲ್ಲಿ ಪಟ್ಟಿ ಮಾಡಲು ಅನುಮೋದಿಸಲಾಗಿದೆ.
ಸೂಚನೆಗಳು: ಕ್ಷೀಣಗೊಳ್ಳುವ ಮೊಣಕಾಲಿನ ಸಂಧಿವಾತದ ಚಿಕಿತ್ಸೆಗಾಗಿ.
ಟೀಕೆಗಳು: Invossa-K ಮಾನವನ ಕೊಂಡ್ರೊಸೈಟ್ಗಳನ್ನು ಒಳಗೊಂಡ ಅಲೋಜೆನಿಕ್ ಸೆಲ್ ಜೀನ್ ಚಿಕಿತ್ಸೆಯಾಗಿದೆ.ಅಲೋಜೆನಿಕ್ ಕೋಶಗಳನ್ನು ವಿಟ್ರೊದಲ್ಲಿ ತಳೀಯವಾಗಿ ಮಾರ್ಪಡಿಸಲಾಗಿದೆ, ಮತ್ತು ಮಾರ್ಪಡಿಸಿದ ಜೀವಕೋಶಗಳು ಒಳ-ಕೀಲಿನ ಇಂಜೆಕ್ಷನ್ ನಂತರ ರೂಪಾಂತರಗೊಳ್ಳುವ ಬೆಳವಣಿಗೆಯ ಅಂಶ β1 (TGF-β1) ಅನ್ನು ವ್ಯಕ್ತಪಡಿಸಬಹುದು ಮತ್ತು ಸ್ರವಿಸಬಹುದು.β1), ಇದರಿಂದಾಗಿ ಅಸ್ಥಿಸಂಧಿವಾತದ ಲಕ್ಷಣಗಳನ್ನು ಸುಧಾರಿಸುತ್ತದೆ.ಇನ್ವೊಸ್ಸಾ-ಕೆ ಮೊಣಕಾಲಿನ ಸಂಧಿವಾತವನ್ನು ಗಮನಾರ್ಹವಾಗಿ ಸುಧಾರಿಸುತ್ತದೆ ಎಂದು ಕ್ಲಿನಿಕಲ್ ಫಲಿತಾಂಶಗಳು ತೋರಿಸುತ್ತವೆ.ಇದನ್ನು 2019 ರಲ್ಲಿ ಕೊರಿಯನ್ ಆಹಾರ ಮತ್ತು ಔಷಧ ಆಡಳಿತವು ಹಿಂತೆಗೆದುಕೊಂಡಿತು ಏಕೆಂದರೆ ತಯಾರಕರು ಬಳಸಿದ ಪದಾರ್ಥಗಳನ್ನು ತಪ್ಪಾಗಿ ಲೇಬಲ್ ಮಾಡಿದ್ದಾರೆ.
(4) ಜಿಂಟೆಗ್ಲೋ
ಕಂಪನಿ: ಬ್ಲೂಬರ್ಡ್ ಬಯೋದಿಂದ ಸಂಶೋಧನೆ ಮತ್ತು ಅಭಿವೃದ್ಧಿಪಡಿಸಲಾಗಿದೆ.
ಮಾರುಕಟ್ಟೆಗೆ ಸಮಯ: 2019 ರಲ್ಲಿ ಮಾರ್ಕೆಟಿಂಗ್ಗಾಗಿ ಯುರೋಪಿಯನ್ ಯೂನಿಯನ್ನಿಂದ ಅನುಮೋದಿಸಲಾಗಿದೆ ಮತ್ತು ಆಗಸ್ಟ್ 2022 ರಲ್ಲಿ ಯುನೈಟೆಡ್ ಸ್ಟೇಟ್ಸ್ನಲ್ಲಿ ಮಾರ್ಕೆಟಿಂಗ್ಗಾಗಿ FDA ಯಿಂದ ಅನುಮೋದಿಸಲಾಗಿದೆ.
ಸೂಚನೆಗಳು: ವರ್ಗಾವಣೆ-ಅವಲಂಬಿತ β-ಥಲಸ್ಸೆಮಿಯಾ ಚಿಕಿತ್ಸೆಗಾಗಿ.
ಟೀಕೆಗಳು: Zynteglo ಒಂದು ಲೆಂಟಿವೈರಲ್ ಇನ್ ವಿಟ್ರೊ ಜೀನ್ ಥೆರಪಿ ಆಗಿದ್ದು, ಇದು ಸಾಮಾನ್ಯ β-ಗ್ಲೋಬಿನ್ ಜೀನ್ನ (βA-T87Q-ಗ್ಲೋಬಿನ್ ಜೀನ್) ಕ್ರಿಯಾತ್ಮಕ ನಕಲನ್ನು ರೋಗಿಯಿಂದ ಲೆಂಟಿವೈರಲ್ ವೆಕ್ಟರ್ ಮೂಲಕ ತೆಗೆದುಕೊಳ್ಳಲಾದ ಹೆಮಟೊಪಯಟಿಕ್ ಸ್ಟೆಮ್ ಸೆಲ್ಗಳಿಗೆ ಪರಿಚಯಿಸುತ್ತದೆ ಮತ್ತು ನಂತರ ಈ ಆನುವಂಶಿಕವಾಗಿ ಮಾರ್ಪಡಿಸಿದ ರೋಗಿಗೆ ಮರುಹೊಂದಿಸುತ್ತದೆ.ರೋಗಿಯು ಒಮ್ಮೆ ಸಾಮಾನ್ಯ βA-T87Q-ಗ್ಲೋಬಿನ್ ಜೀನ್ ಅನ್ನು ಹೊಂದಿದ್ದರೆ, ಅವರು ಸಾಮಾನ್ಯ HbAT87Q ಪ್ರೋಟೀನ್ ಅನ್ನು ಉತ್ಪಾದಿಸಬಹುದು, ಇದು ರಕ್ತ ವರ್ಗಾವಣೆಯ ಅಗತ್ಯವನ್ನು ಪರಿಣಾಮಕಾರಿಯಾಗಿ ಕಡಿಮೆ ಮಾಡುತ್ತದೆ ಅಥವಾ ತೆಗೆದುಹಾಕುತ್ತದೆ.ಇದು 12 ವರ್ಷ ಮತ್ತು ಅದಕ್ಕಿಂತ ಹೆಚ್ಚಿನ ವಯಸ್ಸಿನ ರೋಗಿಗಳಿಗೆ ಜೀವಮಾನದ ರಕ್ತ ವರ್ಗಾವಣೆ ಮತ್ತು ಜೀವಮಾನದ ಔಷಧಿಗಳನ್ನು ಬದಲಿಸಲು ವಿನ್ಯಾಸಗೊಳಿಸಲಾದ ಒಂದು-ಬಾರಿ ಚಿಕಿತ್ಸೆಯಾಗಿದೆ.
(5) ಸ್ಕೈಸೋನಾ
ಕಂಪನಿ: ಬ್ಲೂಬರ್ಡ್ ಬಯೋದಿಂದ ಸಂಶೋಧನೆ ಮತ್ತು ಅಭಿವೃದ್ಧಿಪಡಿಸಲಾಗಿದೆ.
ಮಾರುಕಟ್ಟೆಗೆ ಸಮಯ: ಜುಲೈ 2021 ರಲ್ಲಿ ಮಾರ್ಕೆಟಿಂಗ್ಗಾಗಿ ಯುರೋಪಿಯನ್ ಯೂನಿಯನ್ನಿಂದ ಅನುಮೋದಿಸಲಾಗಿದೆ ಮತ್ತು ಸೆಪ್ಟೆಂಬರ್ 2022 ರಲ್ಲಿ ಯುನೈಟೆಡ್ ಸ್ಟೇಟ್ಸ್ನಲ್ಲಿ ಮಾರ್ಕೆಟಿಂಗ್ ಮಾಡಲು FDA ಯಿಂದ ಅನುಮೋದಿಸಲಾಗಿದೆ.
ಸೂಚನೆಗಳು: ಆರಂಭಿಕ ಸೆರೆಬ್ರಲ್ ಅಡ್ರಿನೊಲ್ಯುಕೋಡಿಸ್ಟ್ರೋಫಿ (ಸಿಎಎಲ್ಡಿ) ಚಿಕಿತ್ಸೆಗಾಗಿ.
ಟೀಕೆಗಳು: ಸ್ಕೈಸೋನಾ ಜೀನ್ ಚಿಕಿತ್ಸೆಯು ಆರಂಭಿಕ ಹಂತದ ಸೆರೆಬ್ರಲ್ ಅಡ್ರಿನೊಲ್ಯುಕೋಡಿಸ್ಟ್ರೋಫಿ (CALD) ಚಿಕಿತ್ಸೆಗಾಗಿ ಅನುಮೋದಿಸಲಾದ ಏಕೈಕ ಜೀನ್ ಚಿಕಿತ್ಸೆಯಾಗಿದೆ.ಸ್ಕೈಸೋನಾ (ಎಲಿವಾಲ್ಡೋಜೆನ್ ಆಟೋಟೆಮ್ಸೆಲ್, ಲೆಂಟಿ-ಡಿ) ಒಂದು ಹೆಮಟೊಪಯಟಿಕ್ ಸ್ಟೆಮ್ ಸೆಲ್ ಲೆಂಟಿವೈರಲ್ ಇನ್ ವಿಟ್ರೊ ಜೀನ್ ಥೆರಪಿ ಲೆಂಟಿ-ಡಿ.ಚಿಕಿತ್ಸೆಯ ಸಾಮಾನ್ಯ ವಿಧಾನವು ಈ ಕೆಳಗಿನಂತಿರುತ್ತದೆ: ರೋಗಿಯಿಂದ ಆಟೋಲೋಗಸ್ ಹೆಮಾಟೊಪಯಟಿಕ್ ಕಾಂಡಕೋಶಗಳನ್ನು ಹೊರತೆಗೆಯಲಾಗುತ್ತದೆ, ಮಾನವನ ABCD1 ಜೀನ್ ಅನ್ನು ವಿಟ್ರೊದಲ್ಲಿ ಸಾಗಿಸುವ ಲೆಂಟಿವೈರಸ್ ಮೂಲಕ ರವಾನಿಸಲಾಗುತ್ತದೆ ಮತ್ತು ಮಾರ್ಪಡಿಸಲಾಗುತ್ತದೆ ಮತ್ತು ನಂತರ ರೋಗಿಗೆ ಪುನಃ ತುಂಬಿಸಲಾಗುತ್ತದೆ.ಇದನ್ನು 18 ವರ್ಷಕ್ಕಿಂತ ಕಡಿಮೆ ವಯಸ್ಸಿನ ರೋಗಿಗಳಿಗೆ ಚಿಕಿತ್ಸೆ ನೀಡಲು ಬಳಸಲಾಗುತ್ತದೆ, ABCD1 ಜೀನ್ ರೂಪಾಂತರಗಳು ಮತ್ತು CALD.
(6) ಕಿಮ್ರಿಯಾ
ಕಂಪನಿ: ನೊವಾರ್ಟಿಸ್ನಿಂದ ಅಭಿವೃದ್ಧಿಪಡಿಸಲಾಗಿದೆ.
ಮಾರುಕಟ್ಟೆಗೆ ಸಮಯ: ಆಗಸ್ಟ್ 2017 ರಲ್ಲಿ ಮಾರ್ಕೆಟಿಂಗ್ಗಾಗಿ FDA ಯಿಂದ ಅನುಮೋದಿಸಲಾಗಿದೆ.
ಸೂಚನೆಗಳು: ಪೂರ್ವಗಾಮಿ ಬಿ-ಸೆಲ್ ಅಕ್ಯೂಟ್ ಲಿಂಫೋಬ್ಲಾಸ್ಟಿಕ್ ಲ್ಯುಕೇಮಿಯಾ (ಎಎಲ್ಎಲ್) ಮತ್ತು ಮರುಕಳಿಸಿದ ಮತ್ತು ರಿಫ್ರ್ಯಾಕ್ಟರಿ ಡಿಎಲ್ಬಿಸಿಎಲ್ ಚಿಕಿತ್ಸೆ.
ಟೀಕೆಗಳು: ಕಿಮ್ರಿಯಾವು ಲೆಂಟಿವೈರಲ್ ಇನ್ ವಿಟ್ರೊ ಜೀನ್ ಥೆರಪಿ ಡ್ರಗ್ ಆಗಿದೆ, ಇದು ವಿಶ್ವದ ಮಾರ್ಕೆಟಿಂಗ್ಗಾಗಿ ಅನುಮೋದಿಸಲಾದ ಮೊದಲ CAR-T ಚಿಕಿತ್ಸೆಯಾಗಿದೆ, ಇದು CD19 ಅನ್ನು ಗುರಿಯಾಗಿಸುತ್ತದೆ ಮತ್ತು 4-1BB ಸಹ-ಪ್ರಚೋದಕ ಅಂಶವನ್ನು ಬಳಸುತ್ತದೆ.ಇದರ ಬೆಲೆ US ನಲ್ಲಿ $475,000 ಮತ್ತು ಜಪಾನ್ನಲ್ಲಿ $313,000.
(7) ಯೆಸ್ಕಾರ್ಟಾ
ಕಂಪನಿ: ಗಿಲಿಯಾಡ್ (GILD) ನ ಅಂಗಸಂಸ್ಥೆಯಾದ ಕೈಟ್ ಫಾರ್ಮಾದಿಂದ ಅಭಿವೃದ್ಧಿಪಡಿಸಲಾಗಿದೆ.
ಮಾರುಕಟ್ಟೆಗೆ ಸಮಯ: ಅಕ್ಟೋಬರ್ 2017 ರಲ್ಲಿ ಮಾರ್ಕೆಟಿಂಗ್ಗಾಗಿ FDA ಯಿಂದ ಅನುಮೋದಿಸಲಾಗಿದೆ;ಫೋಸನ್ ಕೈಟ್ ಕೈಟ್ ಫಾರ್ಮಾದಿಂದ ಯೆಸ್ಕಾರ್ಟಾ ತಂತ್ರಜ್ಞಾನವನ್ನು ಪರಿಚಯಿಸಿತು ಮತ್ತು ಅಧಿಕೃತತೆಯನ್ನು ಪಡೆದ ನಂತರ ಅದನ್ನು ಚೀನಾದಲ್ಲಿ ಉತ್ಪಾದಿಸಿತು.ದೇಶದಲ್ಲಿ ಪಟ್ಟಿ ಮಾಡಲು ಅನುಮೋದಿಸಲಾಗಿದೆ.
ಸೂಚನೆಗಳು: ಮರುಕಳಿಸಿದ ಅಥವಾ ವಕ್ರೀಭವನದ ದೊಡ್ಡ ಬಿ-ಸೆಲ್ ಲಿಂಫೋಮಾದ ಚಿಕಿತ್ಸೆಗಾಗಿ.
ಟೀಕೆಗಳು: ಯೆಸ್ಕಾರ್ಟಾವು ರೆಟ್ರೋವೈರಲ್ ಇನ್ ವಿಟ್ರೊ ಜೀನ್ ಥೆರಪಿಯಾಗಿದೆ, ಇದು ವಿಶ್ವದ ಎರಡನೇ ಅನುಮೋದಿತ CAR-T ಚಿಕಿತ್ಸೆಯಾಗಿದೆ.ಇದು CD19 ಅನ್ನು ಗುರಿಯಾಗಿಸುತ್ತದೆ ಮತ್ತು CD28 ನ ಕಾಸ್ಟಿಮ್ಯುಲೇಟರ್ ಅನ್ನು ಅಳವಡಿಸಿಕೊಂಡಿದೆ.ಯುನೈಟೆಡ್ ಸ್ಟೇಟ್ಸ್ನಲ್ಲಿ ಇದರ ಬೆಲೆ $373,000.
(8) ಟೆಕಾರ್ಟಸ್
ಕಂಪನಿ: ಗಿಲಿಯಾಡ್ (GILD) ಅಭಿವೃದ್ಧಿಪಡಿಸಿದೆ.
ಮಾರುಕಟ್ಟೆಗೆ ಸಮಯ: ಜುಲೈ 2020 ರಲ್ಲಿ ಮಾರ್ಕೆಟಿಂಗ್ಗಾಗಿ FDA ಯಿಂದ ಅನುಮೋದಿಸಲಾಗಿದೆ.
ಸೂಚನೆಗಳು: ಮರುಕಳಿಸಿದ ಅಥವಾ ವಕ್ರೀಭವನದ ಕವಚದ ಕೋಶ ಲಿಂಫೋಮಾಕ್ಕೆ.
ಟೀಕೆಗಳು: ಟೆಕಾರ್ಟಸ್ CD19 ಅನ್ನು ಗುರಿಯಾಗಿಟ್ಟುಕೊಂಡು ಒಂದು ಆಟೋಲೋಗಸ್ CAR-T ಸೆಲ್ ಥೆರಪಿಯಾಗಿದೆ ಮತ್ತು ಇದು ವಿಶ್ವದಲ್ಲಿ ಮಾರ್ಕೆಟಿಂಗ್ಗಾಗಿ ಅನುಮೋದಿಸಲಾದ ಮೂರನೇ CAR-T ಚಿಕಿತ್ಸೆಯಾಗಿದೆ.
(9) ಬ್ರ್ಯಾಂಜಿ
ಕಂಪನಿ: ಬ್ರಿಸ್ಟಲ್-ಮೈಯರ್ಸ್ ಸ್ಕ್ವಿಬ್ (BMS) ಅಭಿವೃದ್ಧಿಪಡಿಸಿದೆ.
ಮಾರುಕಟ್ಟೆಗೆ ಸಮಯ: ಫೆಬ್ರವರಿ 2021 ರಲ್ಲಿ ಮಾರ್ಕೆಟಿಂಗ್ಗಾಗಿ FDA ಯಿಂದ ಅನುಮೋದಿಸಲಾಗಿದೆ.
ಸೂಚನೆಗಳು: ಮರುಕಳಿಸಿದ ಅಥವಾ ರಿಫ್ರ್ಯಾಕ್ಟರಿ (R/R) ದೊಡ್ಡ B-ಸೆಲ್ ಲಿಂಫೋಮಾ (LBCL).
ಟೀಕೆಗಳು: ಬ್ರೆಯಾಂಜಿಯು ಲೆಂಟಿವೈರಸ್ ಅನ್ನು ಆಧರಿಸಿದ ಇನ್ ವಿಟ್ರೊ ಜೀನ್ ಚಿಕಿತ್ಸೆಯಾಗಿದೆ, ಇದು CD19 ಅನ್ನು ಗುರಿಯಾಗಿಸಿಕೊಂಡು ವಿಶ್ವದಲ್ಲಿ ಮಾರ್ಕೆಟಿಂಗ್ ಮಾಡಲು ಅನುಮೋದಿಸಲಾದ ನಾಲ್ಕನೇ CAR-T ಚಿಕಿತ್ಸೆಯಾಗಿದೆ.ಬ್ರೆಯಾಂಜಿಯ ಅನುಮೋದನೆಯು ಸೆಲ್ಯುಲಾರ್ ಇಮ್ಯುನೊಥೆರಪಿ ಕ್ಷೇತ್ರದಲ್ಲಿ ಬ್ರಿಸ್ಟಲ್-ಮೈಯರ್ಸ್ ಸ್ಕ್ವಿಬ್ಗೆ ಒಂದು ಮೈಲಿಗಲ್ಲಾಗಿದೆ, ಇದು ಸೆಲ್ಜೀನ್ ಅನ್ನು 2019 ರಲ್ಲಿ $74 ಶತಕೋಟಿಗೆ ಸ್ವಾಧೀನಪಡಿಸಿಕೊಂಡಾಗ ಅದನ್ನು ಪಡೆದುಕೊಂಡಿತು.
(10) ಅಬೆಕ್ಮಾ
ಕಂಪನಿ: ಬ್ರಿಸ್ಟಲ್-ಮೈಯರ್ಸ್ ಸ್ಕ್ವಿಬ್ (BMS) ಮತ್ತು ಬ್ಲೂಬರ್ಡ್ ಬಯೋದಿಂದ ಸಹ-ಅಭಿವೃದ್ಧಿಪಡಿಸಲಾಗಿದೆ.
ಮಾರುಕಟ್ಟೆಗೆ ಸಮಯ: ಮಾರ್ಚ್ 2021 ರಲ್ಲಿ ಮಾರ್ಕೆಟಿಂಗ್ಗಾಗಿ FDA ಯಿಂದ ಅನುಮೋದಿಸಲಾಗಿದೆ.
ಸೂಚನೆಗಳು: ಮರುಕಳಿಸುವ ಅಥವಾ ವಕ್ರೀಭವನದ ಬಹು ಮೈಲೋಮಾ.
ಟೀಕೆಗಳು: ಅಬೆಕ್ಮಾ ಲೆಂಟಿವೈರಸ್ ಅನ್ನು ಆಧರಿಸಿದ ಇನ್ ವಿಟ್ರೊ ಜೀನ್ ಚಿಕಿತ್ಸೆಯಾಗಿದೆ, ಇದು BCMA ಅನ್ನು ಗುರಿಯಾಗಿಸುವ ವಿಶ್ವದ ಮೊದಲ CAR-T ಸೆಲ್ ಥೆರಪಿ ಮತ್ತು FDA ಯಿಂದ ಅನುಮೋದಿಸಲಾದ ಐದನೇ CAR-T ಚಿಕಿತ್ಸೆಯಾಗಿದೆ.ವಿಟ್ರೊದಲ್ಲಿ ಲೆಂಟಿವೈರಸ್-ಮಧ್ಯಸ್ಥ ಜೀನ್ ಮಾರ್ಪಾಡು ಮೂಲಕ ರೋಗಿಯ ಸ್ವಂತ T ಜೀವಕೋಶಗಳ ಮೇಲೆ ಚಿಮೆರಿಕ್ BCMA ಗ್ರಾಹಕಗಳನ್ನು ವ್ಯಕ್ತಪಡಿಸುವುದು ಔಷಧದ ತತ್ವವಾಗಿದೆ.ರೋಗಿಗಳಲ್ಲಿ ತಳೀಯವಾಗಿ ಮಾರ್ಪಡಿಸದ T ಕೋಶಗಳನ್ನು ತೊಡೆದುಹಾಕಲು ಚಿಕಿತ್ಸೆ, ಮತ್ತು ನಂತರ ಮಾರ್ಪಡಿಸಿದ T ಜೀವಕೋಶಗಳನ್ನು ಪುನಃ ತುಂಬಿಸುತ್ತದೆ, ಇದು ರೋಗಿಗಳಲ್ಲಿ BCMA- ವ್ಯಕ್ತಪಡಿಸುವ ಕ್ಯಾನ್ಸರ್ ಕೋಶಗಳನ್ನು ಹುಡುಕುತ್ತದೆ ಮತ್ತು ಕೊಲ್ಲುತ್ತದೆ.
(11) ಲಿಬ್ಮೆಲ್ಡಿ
ಕಂಪನಿ: ಆರ್ಚರ್ಡ್ ಥೆರಪ್ಯೂಟಿಕ್ಸ್ ಅಭಿವೃದ್ಧಿಪಡಿಸಿದೆ.
ಮಾರುಕಟ್ಟೆಗೆ ಸಮಯ: ಡಿಸೆಂಬರ್ 2020 ರಲ್ಲಿ ಪಟ್ಟಿ ಮಾಡಲು ಯುರೋಪಿಯನ್ ಒಕ್ಕೂಟದಿಂದ ಅನುಮೋದಿಸಲಾಗಿದೆ.
ಸೂಚನೆಗಳು: ಮೆಟಾಕ್ರೊಮ್ಯಾಟಿಕ್ ಲ್ಯುಕೋಡಿಸ್ಟ್ರೋಫಿ (MLD) ಚಿಕಿತ್ಸೆಗಾಗಿ.
ಟೀಕೆಗಳು: ಲಿಬ್ಮೆಲ್ಡಿ ಎಂಬುದು ಲೆಂಟಿವೈರಸ್ನಿಂದ ವಿಟ್ರೊದಲ್ಲಿ ತಳೀಯವಾಗಿ ಮಾರ್ಪಡಿಸಲಾದ ಆಟೋಲೋಗಸ್ CD34+ ಕೋಶಗಳನ್ನು ಆಧರಿಸಿದ ಜೀನ್ ಚಿಕಿತ್ಸೆಯಾಗಿದೆ.ಅದೇ ವಯಸ್ಸಿನ ಚಿಕಿತ್ಸೆ ಪಡೆಯದ ರೋಗಿಗಳಲ್ಲಿ ತೀವ್ರವಾದ ಮೋಟಾರ್ ಮತ್ತು ಅರಿವಿನ ದುರ್ಬಲತೆಗೆ ಹೋಲಿಸಿದರೆ ಲಿಬ್ಮೆಲ್ಡಿಯ ಒಂದು ಇಂಟ್ರಾವೆನಸ್ ಇನ್ಫ್ಯೂಷನ್ ಆರಂಭಿಕ-ಆರಂಭದ MLD ಯ ಕೋರ್ಸ್ ಅನ್ನು ಪರಿಣಾಮಕಾರಿಯಾಗಿ ಬದಲಾಯಿಸುತ್ತದೆ ಎಂದು ಕ್ಲಿನಿಕಲ್ ಡೇಟಾ ತೋರಿಸುತ್ತದೆ.
(12) ಬೆನೋಡಾ
ಕಂಪನಿ: WuXi ಜೈಂಟ್ ನುವೋ ಅಭಿವೃದ್ಧಿಪಡಿಸಿದ್ದಾರೆ.
ಮಾರುಕಟ್ಟೆಗೆ ಸಮಯ: ಸೆಪ್ಟೆಂಬರ್ 2021 ರಲ್ಲಿ NMPA ನಿಂದ ಅಧಿಕೃತವಾಗಿ ಅನುಮೋದಿಸಲಾಗಿದೆ.
ಸೂಚನೆಗಳು: ಎರಡನೇ ಸಾಲಿನ ಅಥವಾ ಅದಕ್ಕಿಂತ ಹೆಚ್ಚಿನ ವ್ಯವಸ್ಥಿತ ಚಿಕಿತ್ಸೆಯ ನಂತರ ಮರುಕಳಿಸುವ ಅಥವಾ ವಕ್ರೀಭವನದ ದೊಡ್ಡ ಬಿ-ಸೆಲ್ ಲಿಂಫೋಮಾ (r/r LBCL) ಹೊಂದಿರುವ ವಯಸ್ಕ ರೋಗಿಗಳ ಚಿಕಿತ್ಸೆ.
ಟೀಕೆಗಳು: Beinoda ವಿರೋಧಿ CD19 CAR-T ಜೀನ್ ಚಿಕಿತ್ಸೆಯಾಗಿದೆ, ಮತ್ತು ಇದು WuXi Juro ಕಂಪನಿಯ ಪ್ರಮುಖ ಉತ್ಪನ್ನವಾಗಿದೆ.ಇದು ಚೀನಾದಲ್ಲಿ ಅನುಮೋದಿಸಲಾದ ಎರಡನೇ CAR-T ಉತ್ಪನ್ನವಾಗಿದೆ, ಮರುಕಳಿಸಿದ/ವಕ್ರೀಭವನದ ದೊಡ್ಡ B-ಸೆಲ್ ಲಿಂಫಾಯಿಡ್ WuXi ದೈತ್ಯ Nuo ಸಹ ಫೋಲಿಕ್ಯುಲಾರ್ ಲಿಂಫೋಮಾ (FL), ಮ್ಯಾಂಟಲ್ ಸೆಲ್ ಲಿಂಫೋಮಾ (MCL), ದೊಡ್ಡ ಕೋಶ ಲಿಂಫೋಮಾ (MCL, ದೀರ್ಘಾವಧಿಯ lymphocytic) ಎಲ್ಎಲ್ಎಲ್ ಸೇರಿದಂತೆ ಅನೇಕ ಇತರ ಸೂಚನೆಗಳ ಚಿಕಿತ್ಸೆಗಾಗಿ Regiorensai ಇಂಜೆಕ್ಷನ್ ಅನ್ನು ಅಭಿವೃದ್ಧಿಪಡಿಸಲು ಯೋಜಿಸಿದೆ. ಲಿಂಫೋಮಾ (DLBCL) ಮತ್ತು ತೀವ್ರವಾದ ಲಿಂಫೋಬ್ಲಾಸ್ಟಿಕ್ ಲ್ಯುಕೇಮಿಯಾ (ALL).
(13) ಕಾರ್ವಿಕ್ತಿ
ಕಂಪನಿ: ಲೆಜೆಂಡ್ ಬಯೋಟೆಕ್ನ ಮೊದಲ ಉತ್ಪನ್ನವನ್ನು ಮಾರುಕಟ್ಟೆಗೆ ಅನುಮೋದಿಸಲಾಗಿದೆ.
ಮಾರುಕಟ್ಟೆಗೆ ಸಮಯ: ಫೆಬ್ರವರಿ 2022 ರಲ್ಲಿ ಮಾರ್ಕೆಟಿಂಗ್ಗಾಗಿ FDA ಯಿಂದ ಅನುಮೋದಿಸಲಾಗಿದೆ.
ಸೂಚನೆಗಳು: ಮರುಕಳಿಸಿದ ಅಥವಾ ರಿಫ್ರ್ಯಾಕ್ಟರಿ ಮಲ್ಟಿಪಲ್ ಮೈಲೋಮಾ (R/R MM) ಚಿಕಿತ್ಸೆಗಾಗಿ.
ಟೀಕೆಗಳು: CARVYKTI (ಸಿಲ್ಟಾಕ್ಯಾಬ್ಟಾಜೆನ್ ಆಟೊಲ್ಯೂಸೆಲ್, ಸಿಲ್ಟಾ-ಸೆಲ್ ಸಂಕ್ಷಿಪ್ತವಾಗಿ) ಎಂಬುದು CAR-T ಜೀವಕೋಶದ ಪ್ರತಿರಕ್ಷಣಾ ಜೀನ್ ಚಿಕಿತ್ಸೆಯಾಗಿದ್ದು, B-ಕೋಶ ಪಕ್ವತೆಯ ಪ್ರತಿಜನಕವನ್ನು (BCMA) ಗುರಿಪಡಿಸುವ ಎರಡು ಏಕ-ಡೊಮೈನ್ ಪ್ರತಿಕಾಯಗಳನ್ನು ಹೊಂದಿದೆ.ನಾಲ್ಕು ಅಥವಾ ಅದಕ್ಕಿಂತ ಹೆಚ್ಚು ಮುಂಚಿನ ಚಿಕಿತ್ಸೆಗಳನ್ನು ಪಡೆದ (ಪ್ರೋಟಿಸೋಮ್ ಇನ್ಹಿಬಿಟರ್ಗಳು, ಇಮ್ಯುನೊಮಾಡ್ಯುಲೇಟರ್ಗಳು ಮತ್ತು ಆಂಟಿ-ಸಿಡಿ 38 ಮೊನೊಕ್ಲೋನಲ್ ಪ್ರತಿಕಾಯಗಳು ಸೇರಿದಂತೆ) ಮರುಕಳಿಸಿದ ಅಥವಾ ವಕ್ರೀಭವನದ ಮಲ್ಟಿಪಲ್ ಮೈಲೋಮಾ ಹೊಂದಿರುವ ರೋಗಿಗಳಲ್ಲಿ 98% ರ ಒಟ್ಟಾರೆ ಪ್ರತಿಕ್ರಿಯೆ ದರವನ್ನು ತೋರಿಸಲಾಗಿದೆ ಎಂದು ಡೇಟಾ ತೋರಿಸುತ್ತದೆ.
(14)ಎಬ್ವಾಲ್ಲೋ
ಕಂಪನಿ: ಅಟಾರಾ ಬಯೋಥೆರಪಿಟಿಕ್ಸ್ನಿಂದ ಅಭಿವೃದ್ಧಿಪಡಿಸಲಾಗಿದೆ.
ಡಿಸೆಂಬರ್ 2022 ರಲ್ಲಿ ಮಾರ್ಕೆಟಿಂಗ್ಗಾಗಿ ಯುರೋಪಿಯನ್ ಕಮಿಷನ್ (EC), ಇದು ಮಾರ್ಕೆಟಿಂಗ್ಗಾಗಿ ಅನುಮೋದಿಸಲಾದ ವಿಶ್ವದ ಮೊದಲ ಸಾರ್ವತ್ರಿಕ ಟಿ ಸೆಲ್ ಚಿಕಿತ್ಸೆಯಾಗಿದೆ.
ಸೂಚನೆಗಳು: ಎಪ್ಸ್ಟೀನ್-ಬಾರ್ ವೈರಸ್ (ಇಬಿವಿ)-ಸಂಬಂಧಿತ ಪೋಸ್ಟ್-ಟ್ರಾನ್ಸ್ಪ್ಲಾಂಟೇಶನ್ ಲಿಂಫೋಪ್ರೊಲಿಫೆರೇಟಿವ್ ಡಿಸೀಸ್ (ಇಬಿವಿ + ಪಿಟಿಎಲ್ಡಿ) ಗಾಗಿ ಮೊನೊಥೆರಪಿಯಾಗಿ, ಚಿಕಿತ್ಸೆ ಪಡೆಯುವ ರೋಗಿಗಳು ವಯಸ್ಕರು ಮತ್ತು 2 ವರ್ಷಕ್ಕಿಂತ ಮೇಲ್ಪಟ್ಟ ಮಕ್ಕಳು ಈ ಹಿಂದೆ ಕನಿಷ್ಠ ಒಂದು ಔಷಧ ಚಿಕಿತ್ಸೆಯನ್ನು ಪಡೆದಿರಬೇಕು.
ಟೀಕೆಗಳು: Ebvallo ಒಂದು ಅಲೋಜೆನಿಕ್ EBV-ನಿರ್ದಿಷ್ಟ ಸಾರ್ವತ್ರಿಕ T-ಕೋಶ ಜೀನ್ ಚಿಕಿತ್ಸೆಯಾಗಿದ್ದು ಅದು HLA-ನಿರ್ಬಂಧಿತ ರೀತಿಯಲ್ಲಿ EBV-ಸೋಂಕಿತ ಕೋಶಗಳನ್ನು ಗುರಿಯಾಗಿಸುತ್ತದೆ ಮತ್ತು ತೆಗೆದುಹಾಕುತ್ತದೆ.ಈ ಚಿಕಿತ್ಸೆಯ ಅನುಮೋದನೆಯು ಪ್ರಮುಖ ಹಂತ 3 ಕ್ಲಿನಿಕಲ್ ಪ್ರಯೋಗ ಅಧ್ಯಯನದ ಫಲಿತಾಂಶಗಳನ್ನು ಆಧರಿಸಿದೆ, ಮತ್ತು ಫಲಿತಾಂಶಗಳು HCT ಗುಂಪು ಮತ್ತು SOT ಗುಂಪಿನ ORR 50% ಎಂದು ತೋರಿಸಿದೆ.ಸಂಪೂರ್ಣ ಉಪಶಮನ (CR) ದರವು 26.3%, ಭಾಗಶಃ ಉಪಶಮನ (PR) ದರವು 23.7%, ಮತ್ತು ಉಪಶಮನಕ್ಕೆ (TTR) ಸರಾಸರಿ ಸಮಯ 1.1 ತಿಂಗಳುಗಳು.ಉಪಶಮನವನ್ನು ಸಾಧಿಸಿದ 19 ರೋಗಿಗಳಲ್ಲಿ, 11 ಜನರು 6 ತಿಂಗಳಿಗಿಂತ ಹೆಚ್ಚು ಪ್ರತಿಕ್ರಿಯೆಯ ಅವಧಿಯನ್ನು (DOR) ಹೊಂದಿದ್ದರು.ಹೆಚ್ಚುವರಿಯಾಗಿ, ಸುರಕ್ಷತೆಯ ದೃಷ್ಟಿಯಿಂದ, ಗ್ರಾಫ್ಟ್-ವರ್ಸಸ್-ಹೋಸ್ಟ್ ಡಿಸೀಸ್ (GvHD) ಅಥವಾ Ebvallo-ಸಂಬಂಧಿತ ಸೈಟೊಕಿನ್ ಬಿಡುಗಡೆ ಸಿಂಡ್ರೋಮ್ನಂತಹ ಯಾವುದೇ ಪ್ರತಿಕೂಲ ಪ್ರತಿಕ್ರಿಯೆಗಳು ಸಂಭವಿಸಿಲ್ಲ.
2. ವೈರಲ್ ವಾಹಕಗಳ ಆಧಾರದ ಮೇಲೆ ವಿವೋ ಜೀನ್ ಚಿಕಿತ್ಸೆಯಲ್ಲಿ
(1) ಜೆಂಡಿಸಿನ್/ಜಿನ್ ಶೆಂಗ್
ಕಂಪನಿ: ಶೆನ್ಜೆನ್ ಸೈಬೈನುವೊ ಕಂಪನಿಯಿಂದ ಅಭಿವೃದ್ಧಿಪಡಿಸಲಾಗಿದೆ.
ಮಾರುಕಟ್ಟೆಗೆ ಸಮಯ: 2003 ರಲ್ಲಿ ಚೀನಾದಲ್ಲಿ ಪಟ್ಟಿ ಮಾಡಲು ಅನುಮೋದಿಸಲಾಗಿದೆ.
ಸೂಚನೆಗಳು: ತಲೆ ಮತ್ತು ಕುತ್ತಿಗೆಯ ಸ್ಕ್ವಾಮಸ್ ಸೆಲ್ ಕಾರ್ಸಿನೋಮ ಚಿಕಿತ್ಸೆಗಾಗಿ.
ಗಮನಿಸಿ: ರಿಕಾಂಬಿನಂಟ್ ಹ್ಯೂಮನ್ ಪಿ53 ಅಡೆನೊವೈರಸ್ ಇಂಜೆಕ್ಷನ್ ಜೆಂಡಿಸಿನ್/ಜಿನ್ಯೌಶೆಂಗ್ ಎಂಬುದು ಅಡೆನೊವೈರಸ್ ವೆಕ್ಟರ್ ಜೀನ್ ಥೆರಪಿ ಔಷಧವಾಗಿದ್ದು, ಶೆನ್ಜೆನ್ ಸೈಬೈನುವೊ ಕಂಪನಿಯ ಮಾಲೀಕತ್ವದ ಸ್ವತಂತ್ರ ಬೌದ್ಧಿಕ ಆಸ್ತಿ ಹಕ್ಕುಗಳನ್ನು ಹೊಂದಿದೆ.ಹ್ಯೂಮನ್ ಟೈಪ್ 5 ಅಡೆನೊವೈರಸ್ ಮಾನವ ಅಡೆನೊವೈರಸ್ ಪ್ರಕಾರ 5 ರ ಸಂಯೋಜನೆಯಾಗಿದೆ. ಮೊದಲನೆಯದು ಔಷಧದ ವಿರೋಧಿ ಗೆಡ್ಡೆಯ ಪರಿಣಾಮಕ್ಕೆ ಮುಖ್ಯ ರಚನೆಯಾಗಿದೆ ಮತ್ತು ಎರಡನೆಯದು ಮುಖ್ಯವಾಗಿ ವಾಹಕವಾಗಿ ಕಾರ್ಯನಿರ್ವಹಿಸುತ್ತದೆ.ಅಡೆನೊವೈರಸ್ ವೆಕ್ಟರ್ ಚಿಕಿತ್ಸಕ ಜೀನ್ p53 ಅನ್ನು ಗುರಿ ಕೋಶಕ್ಕೆ ಒಯ್ಯುತ್ತದೆ, ಗುರಿ ಕೋಶದಲ್ಲಿ ಟ್ಯೂಮರ್ ಸಪ್ರೆಸರ್ ಜೀನ್ p53 ಅನ್ನು ವ್ಯಕ್ತಪಡಿಸುತ್ತದೆ ಮತ್ತು ಅದರ ಜೀನ್ ಅಭಿವ್ಯಕ್ತಿ ಉತ್ಪನ್ನವು ವಿವಿಧ ಕ್ಯಾನ್ಸರ್-ವಿರೋಧಿ ಜೀನ್ಗಳನ್ನು ನಿಯಂತ್ರಿಸುತ್ತದೆ ಮತ್ತು ವಿವಿಧ ಆಂಕೊಜೆನ್ಗಳ ಚಟುವಟಿಕೆಗಳನ್ನು ಕಡಿಮೆ-ನಿಯಂತ್ರಿಸುತ್ತದೆ.
(2) ರಿಗ್ವಿರ್
ಕಂಪನಿ: ಲಾಟ್ವಿಯಾದ ಲಾಟಿಮಾ ಕಂಪನಿಯಿಂದ ಅಭಿವೃದ್ಧಿಪಡಿಸಲಾಗಿದೆ.
ಪಟ್ಟಿ ಮಾಡುವ ಸಮಯ: 2004 ರಲ್ಲಿ ಲಾಟ್ವಿಯಾದಲ್ಲಿ ಪಟ್ಟಿ ಮಾಡಲು ಅನುಮೋದಿಸಲಾಗಿದೆ.
ಸೂಚನೆಗಳು: ಮೆಲನೋಮ ಚಿಕಿತ್ಸೆಗಾಗಿ.
ಟೀಕೆಗಳು: ರಿಗ್ವಿರ್ ಒಂದು ತಳೀಯವಾಗಿ ಮಾರ್ಪಡಿಸಿದ ECHO-7 ಎಂಟ್ರೊವೈರಸ್ ವೆಕ್ಟರ್ ಅನ್ನು ಆಧರಿಸಿದ ಜೀನ್ ಚಿಕಿತ್ಸೆಯಾಗಿದೆ.ಪ್ರಸ್ತುತ, ಔಷಧವನ್ನು ಲಾಟ್ವಿಯಾ, ಎಸ್ಟೋನಿಯಾ, ಪೋಲೆಂಡ್, ಅರ್ಮೇನಿಯಾ, ಬೆಲಾರಸ್, ಇತ್ಯಾದಿಗಳಲ್ಲಿ ಅಳವಡಿಸಿಕೊಳ್ಳಲಾಗಿದೆ ಮತ್ತು EU ದೇಶಗಳಲ್ಲಿ EMA ನೋಂದಣಿಗೆ ಒಳಗಾಗುತ್ತಿದೆ.ಕಳೆದ ಹತ್ತು ವರ್ಷಗಳಲ್ಲಿ ಕ್ಲಿನಿಕಲ್ ಪ್ರಕರಣಗಳು ರಿಗ್ವಿರ್ ಆಂಕೊಲಿಟಿಕ್ ವೈರಸ್ ಸುರಕ್ಷಿತ ಮತ್ತು ಪರಿಣಾಮಕಾರಿ ಎಂದು ಸಾಬೀತುಪಡಿಸಿದೆ ಮತ್ತು ಮೆಲನೋಮ ರೋಗಿಗಳ ಬದುಕುಳಿಯುವಿಕೆಯ ಪ್ರಮಾಣವನ್ನು 4-6 ಪಟ್ಟು ಹೆಚ್ಚಿಸಬಹುದು.ಹೆಚ್ಚುವರಿಯಾಗಿ, ಈ ಚಿಕಿತ್ಸೆಯು ಕೊಲೊರೆಕ್ಟಲ್ ಕ್ಯಾನ್ಸರ್, ಮೇದೋಜ್ಜೀರಕ ಗ್ರಂಥಿಯ ಕ್ಯಾನ್ಸರ್, ಮೂತ್ರಕೋಶ ಕ್ಯಾನ್ಸರ್, ಮೂತ್ರಪಿಂಡದ ಕ್ಯಾನ್ಸರ್, ಪ್ರಾಸ್ಟೇಟ್ ಕ್ಯಾನ್ಸರ್, ಶ್ವಾಸಕೋಶದ ಕ್ಯಾನ್ಸರ್, ಗರ್ಭಾಶಯದ ಕ್ಯಾನ್ಸರ್, ಲಿಂಫೋಸಾರ್ಕೋಮಾ, ಇತ್ಯಾದಿ ಸೇರಿದಂತೆ ವಿವಿಧ ರೀತಿಯ ಕ್ಯಾನ್ಸರ್ಗಳಿಗೆ ಸಹ ಅನ್ವಯಿಸುತ್ತದೆ.
(3) ಆಂಕೊರಿನ್
ಕಂಪನಿ: ಶಾಂಘೈ ಸಾನ್ವೀ ಬಯೋಲಾಜಿಕಲ್ ಕಂಪನಿಯಿಂದ ಅಭಿವೃದ್ಧಿಪಡಿಸಲಾಗಿದೆ.
ಮಾರುಕಟ್ಟೆಗೆ ಸಮಯ: 2005 ರಲ್ಲಿ ಚೀನಾದಲ್ಲಿ ಪಟ್ಟಿ ಮಾಡಲು ಅನುಮೋದಿಸಲಾಗಿದೆ.
ಸೂಚನೆಗಳು: ತಲೆ ಮತ್ತು ಕತ್ತಿನ ಗೆಡ್ಡೆಗಳು, ಯಕೃತ್ತಿನ ಕ್ಯಾನ್ಸರ್, ಪ್ಯಾಂಕ್ರಿಯಾಟಿಕ್ ಕ್ಯಾನ್ಸರ್, ಗರ್ಭಕಂಠದ ಕ್ಯಾನ್ಸರ್ ಮತ್ತು ಇತರ ಕ್ಯಾನ್ಸರ್ಗಳ ಚಿಕಿತ್ಸೆ.
ಟೀಕೆಗಳು: ಆಂಕೊರಿನ್ (安科瑞) ಅಡೆನೊವೈರಸ್ ಅನ್ನು ವಾಹಕವಾಗಿ ಬಳಸುವ ಆಂಕೊಲಿಟಿಕ್ ವೈರಸ್ ಜೀನ್ ಥೆರಪಿ ಉತ್ಪನ್ನವಾಗಿದೆ.ಆಂಕೊಲಿಟಿಕ್ ಅಡೆನೊವೈರಸ್ ಅನ್ನು ಪಡೆಯಲಾಗುತ್ತದೆ, ಇದು ನಿರ್ದಿಷ್ಟವಾಗಿ p53 ಜೀನ್ ಕೊರತೆ ಅಥವಾ ಅಸಹಜ ಗೆಡ್ಡೆಗಳಲ್ಲಿ ಪುನರಾವರ್ತಿಸಬಹುದು, ಇದು ಗೆಡ್ಡೆಯ ಕೋಶಗಳ ವಿಘಟನೆಗೆ ಕಾರಣವಾಗುತ್ತದೆ, ಇದರಿಂದಾಗಿ ಗೆಡ್ಡೆಯ ಕೋಶಗಳನ್ನು ಕೊಲ್ಲುತ್ತದೆ.ಸಾಮಾನ್ಯ ಜೀವಕೋಶಗಳಿಗೆ ಹಾನಿಯಾಗದಂತೆ.ವಿವಿಧ ಮಾರಣಾಂತಿಕ ಗೆಡ್ಡೆಗಳಿಗೆ ಅಂಕೆರುಯಿ ಉತ್ತಮ ಸುರಕ್ಷತೆ ಮತ್ತು ಪರಿಣಾಮಕಾರಿತ್ವವನ್ನು ಹೊಂದಿದೆ ಎಂದು ಕ್ಲಿನಿಕಲ್ ಅಧ್ಯಯನಗಳು ತೋರಿಸಿವೆ.
(4) ಗ್ಲೈಬೆರಾ
ಕಂಪನಿ: uniQure ನಿಂದ ಅಭಿವೃದ್ಧಿಪಡಿಸಲಾಗಿದೆ.
ಮಾರುಕಟ್ಟೆಗೆ ಸಮಯ: 2012 ರಲ್ಲಿ ಯುರೋಪ್ನಲ್ಲಿ ಪಟ್ಟಿ ಮಾಡಲು ಅನುಮೋದಿಸಲಾಗಿದೆ.
ಸೂಚನೆಗಳು: ಕಟ್ಟುನಿಟ್ಟಾಗಿ ನಿರ್ಬಂಧಿತ ಕೊಬ್ಬಿನ ಆಹಾರದ ಹೊರತಾಗಿಯೂ ಮೇದೋಜ್ಜೀರಕ ಗ್ರಂಥಿಯ ತೀವ್ರ ಅಥವಾ ಮರುಕಳಿಸುವ ಕಂತುಗಳೊಂದಿಗೆ ಲಿಪೊಪ್ರೋಟೀನ್ ಲಿಪೇಸ್ ಕೊರತೆಯ (LPLD) ಚಿಕಿತ್ಸೆ.
ಟೀಕೆಗಳು: ಗ್ಲೈಬೆರಾ (ಅಲಿಪೊಜೆನ್ ಟಿಪಾರ್ವೊವೆಕ್) ಎಎವಿ ಆಧಾರಿತ ಜೀನ್ ಥೆರಪಿ ಔಷಧವಾಗಿದೆ, ಇದು ಚಿಕಿತ್ಸಕ ವಂಶವಾಹಿ LPL ಅನ್ನು ಸ್ನಾಯುವಿನ ಜೀವಕೋಶಗಳಿಗೆ ರವಾನಿಸಲು AAV ಅನ್ನು ವಾಹಕವಾಗಿ ಬಳಸುತ್ತದೆ, ಇದರಿಂದಾಗಿ ಅನುಗುಣವಾದ ಜೀವಕೋಶಗಳು ನಿರ್ದಿಷ್ಟ ಪ್ರಮಾಣದ ಲಿಪೊಪ್ರೋಟೀನ್ ಲಿಪೇಸ್ ಅನ್ನು ಉತ್ಪಾದಿಸಬಹುದು, ರೋಗವನ್ನು ನಿವಾರಿಸಲು, ಈ ಚಿಕಿತ್ಸೆಯು ದೀರ್ಘಕಾಲದವರೆಗೆ ಪರಿಣಾಮಕಾರಿಯಾಗಿದೆ (ಹಲವು ವರ್ಷಗಳವರೆಗೆ)ಔಷಧವನ್ನು 2017 ರಲ್ಲಿ ಮಾರುಕಟ್ಟೆಯಿಂದ ಹಿಂತೆಗೆದುಕೊಳ್ಳಲಾಯಿತು. ಅದರ ಹಿಂತೆಗೆದುಕೊಳ್ಳುವಿಕೆಯ ಕಾರಣವು ಎರಡು ಅಂಶಗಳಿಗೆ ಸಂಬಂಧಿಸಿರಬಹುದು: ಹೆಚ್ಚಿನ ಬೆಲೆ ಮತ್ತು ಸೀಮಿತ ಮಾರುಕಟ್ಟೆ ಬೇಡಿಕೆ.ಔಷಧದ ಸರಾಸರಿ ಚಿಕಿತ್ಸಾ ವೆಚ್ಚ US$1 ಮಿಲಿಯನ್ನಷ್ಟಿದೆ ಮತ್ತು ಇದುವರೆಗೆ ಒಬ್ಬ ರೋಗಿಯು ಮಾತ್ರ ಅದನ್ನು ಖರೀದಿಸಿ ಬಳಸಿದ್ದಾರೆ.ವೈದ್ಯಕೀಯ ವಿಮಾ ಕಂಪನಿಯು ಅದಕ್ಕಾಗಿ US$900,000 ಮರುಪಾವತಿ ಮಾಡಿದ್ದರೂ, ಇದು ವಿಮಾ ಕಂಪನಿಗೆ ತುಲನಾತ್ಮಕವಾಗಿ ದೊಡ್ಡ ಹೊರೆಯಾಗಿದೆ.ಇದರ ಜೊತೆಗೆ, ಔಷಧವು ಗುರಿಪಡಿಸಿದ ಸೂಚನೆಗಳು ತುಂಬಾ ಅಪರೂಪವಾಗಿದ್ದು, ಸುಮಾರು 1 ಮಿಲಿಯನ್ನಲ್ಲಿ 1 ಘಟನೆಯ ಪ್ರಮಾಣ ಮತ್ತು ಹೆಚ್ಚಿನ ತಪ್ಪು ರೋಗನಿರ್ಣಯದ ಪ್ರಮಾಣವಿದೆ.
(5) ಇಮ್ಲಿಜಿಕ್
ಕಂಪನಿ: ಆಮ್ಜೆನ್ನಿಂದ ಅಭಿವೃದ್ಧಿಪಡಿಸಲಾಗಿದೆ.
ಮಾರುಕಟ್ಟೆಗೆ ಸಮಯ: 2015 ರಲ್ಲಿ, ಇದನ್ನು ಯುನೈಟೆಡ್ ಸ್ಟೇಟ್ಸ್ ಮತ್ತು ಯುರೋಪಿಯನ್ ಒಕ್ಕೂಟದಲ್ಲಿ ಪಟ್ಟಿ ಮಾಡಲು ಅನುಮೋದಿಸಲಾಗಿದೆ.
ಸೂಚನೆಗಳು: ಶಸ್ತ್ರಚಿಕಿತ್ಸೆಯಿಂದ ಸಂಪೂರ್ಣವಾಗಿ ತೆಗೆದುಹಾಕಲಾಗದ ಮೆಲನೋಮ ಗಾಯಗಳ ಚಿಕಿತ್ಸೆ.
ಟೀಕೆಗಳು: ಇಮ್ಲಿಜಿಕ್ ಒಂದು ದುರ್ಬಲಗೊಂಡ ಹರ್ಪಿಸ್ ಸಿಂಪ್ಲೆಕ್ಸ್ ವೈರಸ್ ಟೈಪ್ 1 ಆಗಿದ್ದು, ಇದನ್ನು ಜೆನೆಟಿಕ್ ತಂತ್ರಜ್ಞಾನದಿಂದ ಮಾರ್ಪಡಿಸಲಾಗಿದೆ (ಅದರ ICP34.5 ಮತ್ತು ICP47 ಜೀನ್ ತುಣುಕುಗಳನ್ನು ಅಳಿಸಿ, ಮತ್ತು ಮಾನವ ಗ್ರ್ಯಾನ್ಯುಲೋಸೈಟ್ ಮ್ಯಾಕ್ರೋಫೇಜ್ ಕಾಲೋನಿ-ಉತ್ತೇಜಕ ಅಂಶವನ್ನು ಸೇರಿಸುವುದು GM-CSF ಜೀನ್ ಮೊದಲ ವಂಶವಾಹಿ ಆನ್ಕೊಟಿಕ್ ವೈರಸ್ಗೆ ಎಫ್ಕೋಟಿಕ್ ವೈರಸ್ ಆಗಿದೆ) ಚಿಕಿತ್ಸೆ.ಆಡಳಿತದ ವಿಧಾನವೆಂದರೆ ಇಂಟ್ರಾಲೇಶನಲ್ ಇಂಜೆಕ್ಷನ್, ಇದನ್ನು ನೇರವಾಗಿ ಮೆಲನೋಮಾ ಗಾಯಗಳಿಗೆ ಚುಚ್ಚಲಾಗುತ್ತದೆ, ಇದು ಗೆಡ್ಡೆಯ ಕೋಶಗಳ ಛಿದ್ರವನ್ನು ಉಂಟುಮಾಡುತ್ತದೆ, ಗೆಡ್ಡೆಯಿಂದ ಪಡೆದ ಪ್ರತಿಜನಕಗಳು ಮತ್ತು GM-CSF ಅನ್ನು ಬಿಡುಗಡೆ ಮಾಡುತ್ತದೆ ಮತ್ತು ಆಂಟಿ-ಟ್ಯೂಮರ್ ಪ್ರತಿರಕ್ಷಣಾ ಪ್ರತಿಕ್ರಿಯೆಗಳನ್ನು ಉತ್ತೇಜಿಸುತ್ತದೆ.
(6) ಲಕ್ಸುರ್ನಾ
ಕಂಪನಿ: ರೋಚೆಯ ಅಂಗಸಂಸ್ಥೆಯಾದ ಸ್ಪಾರ್ಕ್ ಥೆರಪ್ಯೂಟಿಕ್ಸ್ ಅಭಿವೃದ್ಧಿಪಡಿಸಿದೆ.
ಮಾರುಕಟ್ಟೆಗೆ ಸಮಯ: ಇದನ್ನು 2017 ರಲ್ಲಿ ಎಫ್ಡಿಎ ಮಾರ್ಕೆಟಿಂಗ್ಗೆ ಅನುಮೋದಿಸಿತು ಮತ್ತು ನಂತರ 2018 ರಲ್ಲಿ ಯುರೋಪ್ನಲ್ಲಿ ಮಾರ್ಕೆಟಿಂಗ್ಗೆ ಅನುಮೋದಿಸಲಾಗಿದೆ.
ಸೂಚನೆಗಳು: ಡಬಲ್-ಕಾಪಿ RPE65 ಜೀನ್ ರೂಪಾಂತರಗಳಿಂದ ದೃಷ್ಟಿ ಕಳೆದುಕೊಂಡಿರುವ ಆದರೆ ಸಾಕಷ್ಟು ಸಂಖ್ಯೆಯ ಕಾರ್ಯಸಾಧ್ಯವಾದ ರೆಟಿನಾದ ಜೀವಕೋಶಗಳನ್ನು ಉಳಿಸಿಕೊಳ್ಳುವ ಮಕ್ಕಳು ಮತ್ತು ವಯಸ್ಕರ ಚಿಕಿತ್ಸೆಗಾಗಿ.
ಟೀಕೆಗಳು: ಲುಕ್ಸ್ಟರ್ನಾ ಎಂಬುದು AAV-ಆಧಾರಿತ ಜೀನ್ ಚಿಕಿತ್ಸೆಯಾಗಿದ್ದು, ಇದನ್ನು ಸಬ್ರೆಟಿನಲ್ ಇಂಜೆಕ್ಷನ್ ಮೂಲಕ ನಿರ್ವಹಿಸಲಾಗುತ್ತದೆ.ಜೀನ್ ಚಿಕಿತ್ಸೆಯು ಸಾಮಾನ್ಯ RPE65 ಜೀನ್ನ ಕ್ರಿಯಾತ್ಮಕ ನಕಲನ್ನು ರೋಗಿಯ ರೆಟಿನಾದ ಜೀವಕೋಶಗಳಿಗೆ ಪರಿಚಯಿಸಲು AAV2 ಅನ್ನು ವಾಹಕವಾಗಿ ಬಳಸುತ್ತದೆ, ಇದರಿಂದಾಗಿ ಅನುಗುಣವಾದ ಜೀವಕೋಶಗಳು ಸಾಮಾನ್ಯ RPE65 ಪ್ರೋಟೀನ್ ಅನ್ನು ವ್ಯಕ್ತಪಡಿಸುತ್ತವೆ, ರೋಗಿಯ RPE65 ಪ್ರೋಟೀನ್ ಕೊರತೆಯನ್ನು ಸರಿದೂಗಿಸುತ್ತದೆ, ಇದರಿಂದಾಗಿ ರೋಗಿಯ ದೃಷ್ಟಿ ಸುಧಾರಿಸುತ್ತದೆ.
(7) ಜೋಲ್ಗೆನ್ಸ್ಮಾ
ಕಂಪನಿ: ನೊವಾರ್ಟಿಸ್ನ ಅಂಗಸಂಸ್ಥೆಯಾದ AveXis ನಿಂದ ಅಭಿವೃದ್ಧಿಪಡಿಸಲಾಗಿದೆ.
ಮಾರುಕಟ್ಟೆಗೆ ಸಮಯ: ಮೇ 2019 ರಲ್ಲಿ ಮಾರ್ಕೆಟಿಂಗ್ಗಾಗಿ FDA ಯಿಂದ ಅನುಮೋದಿಸಲಾಗಿದೆ.
ಸೂಚನೆಗಳು: 2 ವರ್ಷದೊಳಗಿನ ಸ್ಪೈನಲ್ ಮಸ್ಕ್ಯುಲರ್ ಅಟ್ರೋಫಿ (SMA) ರೋಗಿಗಳ ಚಿಕಿತ್ಸೆ.
ಟೀಕೆಗಳು: Zolgensma AAV ವೆಕ್ಟರ್ ಆಧಾರಿತ ಜೀನ್ ಚಿಕಿತ್ಸೆಯಾಗಿದೆ.ಈ ಔಷಧವು ಬೆನ್ನುಮೂಳೆಯ ಸ್ನಾಯುವಿನ ಕ್ಷೀಣತೆಗೆ ಒಂದೇ ಬಾರಿಯ ಚಿಕಿತ್ಸಾ ಯೋಜನೆಯಾಗಿದ್ದು, ಪ್ರಪಂಚದಲ್ಲಿ ಮಾರುಕಟ್ಟೆಗೆ ಅನುಮೋದಿಸಲಾಗಿದೆ.ಔಷಧದ ಉಡಾವಣೆಯು ಬೆನ್ನುಮೂಳೆಯ ಸ್ನಾಯುವಿನ ಕ್ಷೀಣತೆಯ ಚಿಕಿತ್ಸೆಯಲ್ಲಿ ಹೊಸ ಯುಗವನ್ನು ತೆರೆಯುತ್ತದೆ.ಪುಟ, ಒಂದು ಮೈಲಿಗಲ್ಲು ಪ್ರಗತಿಯಾಗಿದೆ.ಈ ಜೀನ್ ಚಿಕಿತ್ಸೆಯು ಸಾಮಾನ್ಯ SMN1 ಪ್ರೋಟೀನ್ ಅನ್ನು ಉತ್ಪಾದಿಸಲು ಇಂಟ್ರಾವೆನಸ್ ಇನ್ಫ್ಯೂಷನ್ ಮೂಲಕ ಸಾಮಾನ್ಯ SMN1 ಜೀನ್ ಅನ್ನು ರೋಗಿಗೆ ಪರಿಚಯಿಸಲು scAAV9 ವೆಕ್ಟರ್ ಅನ್ನು ಬಳಸುತ್ತದೆ, ಇದರಿಂದಾಗಿ ಮೋಟಾರು ನ್ಯೂರಾನ್ಗಳಂತಹ ಪೀಡಿತ ಜೀವಕೋಶಗಳ ಕಾರ್ಯವನ್ನು ಸುಧಾರಿಸುತ್ತದೆ.ಇದಕ್ಕೆ ವ್ಯತಿರಿಕ್ತವಾಗಿ, SMA ಔಷಧಿಗಳಾದ ಸ್ಪಿನ್ರಾಜಾ ಮತ್ತು ಎವ್ರಿಸ್ಡಿ ದೀರ್ಘಾವಧಿಯ ಪುನರಾವರ್ತಿತ ಡೋಸಿಂಗ್ ಅಗತ್ಯವಿರುತ್ತದೆ.ಸ್ಪಿನ್ರಾಜಾವನ್ನು ಪ್ರತಿ ನಾಲ್ಕು ತಿಂಗಳಿಗೊಮ್ಮೆ ಬೆನ್ನುಮೂಳೆಯ ಇಂಜೆಕ್ಷನ್ ಮೂಲಕ ನೀಡಲಾಗುತ್ತದೆ ಮತ್ತು ಎವ್ರಿಸ್ಡಿ ದೈನಂದಿನ ಮೌಖಿಕ ಔಷಧವಾಗಿದೆ.
(8) ಡೆಲಿಟಾಕ್ಟ್
ಕಂಪನಿ: ಡೈಚಿ ಸ್ಯಾಂಕ್ಯೊ ಕಂಪನಿ ಲಿಮಿಟೆಡ್ನಿಂದ ಅಭಿವೃದ್ಧಿಪಡಿಸಲಾಗಿದೆ (TYO: 4568).
ಮಾರುಕಟ್ಟೆಗೆ ಸಮಯ: ಜೂನ್ 2021 ರಲ್ಲಿ ಜಪಾನ್ನ ಆರೋಗ್ಯ, ಕಾರ್ಮಿಕ ಮತ್ತು ಕಲ್ಯಾಣ ಸಚಿವಾಲಯದಿಂದ (MHLW) ಷರತ್ತುಬದ್ಧ ಅನುಮೋದನೆ.
ಸೂಚನೆಗಳು: ಮಾರಣಾಂತಿಕ ಗ್ಲಿಯೋಮಾ ಚಿಕಿತ್ಸೆಗಾಗಿ.
ಟೀಕೆಗಳು: ಡೆಲಿಟಾಕ್ಟ್ ಜಾಗತಿಕವಾಗಿ ಅನುಮೋದಿಸಲಾದ ನಾಲ್ಕನೇ ಆಂಕೊಲಿಟಿಕ್ ವೈರಸ್ ಜೀನ್ ಥೆರಪಿ ಉತ್ಪನ್ನವಾಗಿದೆ ಮತ್ತು ಮಾರಣಾಂತಿಕ ಗ್ಲಿಯೋಮಾ ಚಿಕಿತ್ಸೆಗಾಗಿ ಅನುಮೋದಿಸಲಾದ ಮೊದಲ ಆಂಕೊಲಿಟಿಕ್ ವೈರಸ್ ಉತ್ಪನ್ನವಾಗಿದೆ.ಡೆಲಿಟಾಕ್ಟ್ ಡಾ. ಟೊಡೊ ಮತ್ತು ಸಹೋದ್ಯೋಗಿಗಳು ಅಭಿವೃದ್ಧಿಪಡಿಸಿದ ತಳೀಯವಾಗಿ ವಿನ್ಯಾಸಗೊಳಿಸಿದ ಹರ್ಪಿಸ್ ಸಿಂಪ್ಲೆಕ್ಸ್ ವೈರಸ್ ಟೈಪ್ 1 (HSV-1) ಆಂಕೊಲಿಟಿಕ್ ವೈರಸ್ ಆಗಿದೆ.ಡೆಲಿಟಾಕ್ಟ್ ಎರಡನೇ ತಲೆಮಾರಿನ HSV-1 ನ G207 ಜೀನೋಮ್ಗೆ ಹೆಚ್ಚುವರಿ ಅಳಿಸುವಿಕೆ ರೂಪಾಂತರಗಳನ್ನು ಪರಿಚಯಿಸುತ್ತದೆ, ಕ್ಯಾನ್ಸರ್ ಕೋಶಗಳಲ್ಲಿ ಅದರ ಆಯ್ದ ಪುನರಾವರ್ತನೆಯನ್ನು ಹೆಚ್ಚಿಸುತ್ತದೆ ಮತ್ತು ಹೆಚ್ಚಿನ ಸುರಕ್ಷತೆಯನ್ನು ಕಾಪಾಡಿಕೊಳ್ಳುವಾಗ ಆಂಟಿ-ಟ್ಯೂಮರ್ ಪ್ರತಿರಕ್ಷಣಾ ಪ್ರತಿಕ್ರಿಯೆಗಳ ಪ್ರಚೋದನೆಯನ್ನು ಹೆಚ್ಚಿಸುತ್ತದೆ.ಡೆಲಿಟಾಕ್ಟ್ ಮೊದಲ ಮೂರನೇ ತಲೆಮಾರಿನ ಆಂಕೊಲಿಟಿಕ್ HSV-1 ಪ್ರಸ್ತುತ ವೈದ್ಯಕೀಯ ಮೌಲ್ಯಮಾಪನಕ್ಕೆ ಒಳಗಾಗುತ್ತಿದೆ.ಜಪಾನ್ನಲ್ಲಿ ಡೆಲಿಟಾಕ್ಟ್ನ ಅನುಮೋದನೆಯು ಮುಖ್ಯವಾಗಿ ಸಿಂಗಲ್-ಆರ್ಮ್ ಫೇಸ್ 2 ಕ್ಲಿನಿಕಲ್ ಪ್ರಯೋಗವನ್ನು ಆಧರಿಸಿದೆ.ಮರುಕಳಿಸುವ ಗ್ಲಿಯೊಬ್ಲಾಸ್ಟೊಮಾ ರೋಗಿಗಳಲ್ಲಿ, ಡೆಲಿಟಾಕ್ಟ್ ಒಂದು ವರ್ಷದ ಬದುಕುಳಿಯುವಿಕೆಯ ಪ್ರಾಥಮಿಕ ಅಂತಿಮ ಬಿಂದುವನ್ನು ಸಾಧಿಸಿದೆ ಮತ್ತು ಫಲಿತಾಂಶಗಳು G207 ಗೆ ಹೋಲಿಸಿದರೆ ಡೆಲಿಟಾಕ್ಟ್ ಉತ್ತಮ ಪರಿಣಾಮಕಾರಿತ್ವವನ್ನು ತೋರಿಸಿದೆ.ಬಲವಾದ ಪ್ರತಿಕೃತಿ ಶಕ್ತಿ ಮತ್ತು ಹೆಚ್ಚಿನ ಆಂಟಿಟ್ಯೂಮರ್ ಚಟುವಟಿಕೆ.ಸ್ತನ, ಪ್ರಾಸ್ಟೇಟ್, ಶ್ವಾನ್ನೋಮಾಸ್, ನಾಸೊಫಾರ್ಂಜಿಯಲ್, ಹೆಪಟೊಸೆಲ್ಯುಲರ್, ಕೊಲೊರೆಕ್ಟಲ್, ಮಾರಣಾಂತಿಕ ಬಾಹ್ಯ ನರಗಳ ಪೊರೆ ಗೆಡ್ಡೆಗಳು ಮತ್ತು ಥೈರಾಯ್ಡ್ ಕ್ಯಾನ್ಸರ್ನ ಘನ ಗೆಡ್ಡೆ ಮಾದರಿಗಳಲ್ಲಿ ಇದು ಪರಿಣಾಮಕಾರಿಯಾಗಿದೆ.
(9) ಅಪ್ಸ್ಟಾಜಾ
ಕಂಪನಿ: PTC ಥೆರಪ್ಯೂಟಿಕ್ಸ್, Inc. ಅಭಿವೃದ್ಧಿಪಡಿಸಿದೆ (NASDAQ: PTCT).
ಮಾರುಕಟ್ಟೆಗೆ ಸಮಯ: ಜುಲೈ 2022 ರಲ್ಲಿ ಮಾರ್ಕೆಟಿಂಗ್ಗಾಗಿ ಯುರೋಪಿಯನ್ ಯೂನಿಯನ್ನಿಂದ ಅನುಮೋದಿಸಲಾಗಿದೆ.
ಸೂಚನೆಗಳು: ಆರೊಮ್ಯಾಟಿಕ್ ಎಲ್-ಅಮಿನೊ ಆಸಿಡ್ ಡಿಕಾರ್ಬಾಕ್ಸಿಲೇಸ್ (ಎಎಡಿಸಿ) ಕೊರತೆಗೆ, 18 ತಿಂಗಳ ಮತ್ತು ಅದಕ್ಕಿಂತ ಹೆಚ್ಚಿನ ವಯಸ್ಸಿನ ರೋಗಿಗಳ ಚಿಕಿತ್ಸೆಗಾಗಿ ಇದನ್ನು ಅನುಮೋದಿಸಲಾಗಿದೆ.
ಟೀಕೆಗಳು: Upstaza™ (eladocagene exuparvovec) ಅಡೆನೊ-ಸಂಬಂಧಿತ ವೈರಸ್ ಟೈಪ್ 2 (AAV2) ಅನ್ನು ವಾಹಕವಾಗಿ ಹೊಂದಿರುವ ವಿವೋ ಜೀನ್ ಚಿಕಿತ್ಸೆಯಾಗಿದೆ.AADC ಕಿಣ್ವವನ್ನು ಎನ್ಕೋಡಿಂಗ್ ಮಾಡುವ ಜೀನ್ನಲ್ಲಿನ ರೂಪಾಂತರಗಳಿಂದಾಗಿ ರೋಗಿಗಳು ಅನಾರೋಗ್ಯಕ್ಕೆ ಒಳಗಾಗುತ್ತಾರೆ.AAV2 AADC ಕಿಣ್ವವನ್ನು ಎನ್ಕೋಡಿಂಗ್ ಮಾಡುವ ಆರೋಗ್ಯಕರ ಜೀನ್ ಅನ್ನು ಒಯ್ಯುತ್ತದೆ.ಜೀನ್ ಪರಿಹಾರದ ರೂಪವು ಚಿಕಿತ್ಸಕ ಪರಿಣಾಮವನ್ನು ಸಾಧಿಸುತ್ತದೆ.ಸಿದ್ಧಾಂತದಲ್ಲಿ, ಒಂದು ಆಡಳಿತವು ದೀರ್ಘಕಾಲದವರೆಗೆ ಪರಿಣಾಮಕಾರಿಯಾಗಿದೆ.ಇದು ಮೆದುಳಿಗೆ ನೇರವಾಗಿ ಚುಚ್ಚುಮದ್ದಿನ ಮೊದಲ ಮಾರುಕಟ್ಟೆ ಜೀನ್ ಚಿಕಿತ್ಸೆಯಾಗಿದೆ.ಮಾರ್ಕೆಟಿಂಗ್ ಅಧಿಕಾರವು ಎಲ್ಲಾ 27 EU ಸದಸ್ಯ ರಾಷ್ಟ್ರಗಳಿಗೆ, ಹಾಗೆಯೇ ಐಸ್ಲ್ಯಾಂಡ್, ನಾರ್ವೆ ಮತ್ತು ಲೀಚ್ಟೆನ್ಸ್ಟೈನ್ಗೆ ಅನ್ವಯಿಸುತ್ತದೆ.
(10) ರೊಕ್ಟೇವಿಯನ್
ಕಂಪನಿ: ಬಯೋಮರಿನ್ ಫಾರ್ಮಾಸ್ಯುಟಿಕಲ್ (ಬಯೋಮರಿನ್) ಅಭಿವೃದ್ಧಿಪಡಿಸಿದೆ.
ಮಾರುಕಟ್ಟೆಗೆ ಸಮಯ: ಆಗಸ್ಟ್ 2022 ರಲ್ಲಿ ಯುರೋಪಿಯನ್ ಒಕ್ಕೂಟದಿಂದ ಮಾರ್ಕೆಟಿಂಗ್ಗೆ ಅನುಮೋದಿಸಲಾಗಿದೆ;ನವೆಂಬರ್ 2022 ರಲ್ಲಿ UK ಮೆಡಿಸಿನ್ಸ್ ಮತ್ತು ಹೆಲ್ತ್ಕೇರ್ ಪ್ರಾಡಕ್ಟ್ ಅಡ್ಮಿನಿಸ್ಟ್ರೇಷನ್ (MHRA) ನಿಂದ ಮಾರ್ಕೆಟಿಂಗ್ ದೃಢೀಕರಣ.
ಸೂಚನೆಗಳು: FVIII ಅಂಶದ ಪ್ರತಿಬಂಧದ ಇತಿಹಾಸವನ್ನು ಹೊಂದಿರದ ಮತ್ತು AAV5 ಪ್ರತಿಕಾಯಗಳಿಗೆ ಋಣಾತ್ಮಕವಾಗಿರುವ ತೀವ್ರವಾದ ಹಿಮೋಫಿಲಿಯಾ A ಯ ವಯಸ್ಕ ರೋಗಿಗಳ ಚಿಕಿತ್ಸೆಗಾಗಿ.
ಟೀಕೆಗಳು: ರೊಕ್ಟೇವಿಯನ್ (ವ್ಯಾಲೋಕ್ಟೊಕೊಜೆನ್ ರೋಕ್ಸಾಪರ್ವೊವೆಕ್) AAV5 ಅನ್ನು ವೆಕ್ಟರ್ ಆಗಿ ಬಳಸುತ್ತದೆ ಮತ್ತು B ಡೊಮೇನ್ ಅಳಿಸಲಾದ ಹ್ಯೂಮನ್ ಹೆಪ್ಪುಗಟ್ಟುವಿಕೆ ಅಂಶ VIII (FVIII) ನ ಅಭಿವ್ಯಕ್ತಿಯನ್ನು ಚಾಲನೆ ಮಾಡಲು ಮಾನವ ಯಕೃತ್ತು-ನಿರ್ದಿಷ್ಟ ಪ್ರವರ್ತಕ HLP ಅನ್ನು ಬಳಸುತ್ತದೆ.ವ್ಯಾಲೋಕ್ಟೊಕೊಜೆನ್ ರೊಕ್ಸಾಪರ್ವೊವೆಕ್ನ ಮಾರ್ಕೆಟಿಂಗ್ ಅನ್ನು ಅನುಮೋದಿಸುವ ಯುರೋಪಿಯನ್ ಕಮಿಷನ್ ನಿರ್ಧಾರವು ಔಷಧದ ಕ್ಲಿನಿಕಲ್ ಅಭಿವೃದ್ಧಿ ಯೋಜನೆಯ ಒಟ್ಟಾರೆ ಡೇಟಾವನ್ನು ಆಧರಿಸಿದೆ.ಅವುಗಳಲ್ಲಿ, ಹಂತ III ಕ್ಲಿನಿಕಲ್ ಪ್ರಯೋಗದ ಫಲಿತಾಂಶಗಳು GENER8-1 ದಾಖಲಾತಿಯ ಹಿಂದಿನ ವರ್ಷದ ದತ್ತಾಂಶದೊಂದಿಗೆ ಹೋಲಿಸಿದರೆ, ವ್ಯಾಲೊಕ್ಟೊಕೊಜೆನ್ ರೋಕ್ಸಾಪರ್ವೊವೆಕ್ನ ಒಂದು ಕಷಾಯದ ನಂತರ, ವಿಷಯದ ವಾರ್ಷಿಕ ರಕ್ತಸ್ರಾವದ ಪ್ರಮಾಣ (ABR) ಗಣನೀಯವಾಗಿ ಕಡಿಮೆಯಾಗುತ್ತದೆ, ಮರುಸಂಯೋಜಕ ಬಳಕೆಯ ಆವರ್ತನವು F8 (F8) ರಕ್ತದ ತಯಾರಿಕೆಯಲ್ಲಿ ಗಣನೀಯವಾಗಿ ಹೆಚ್ಚಿದ ಹೆಪ್ಪುಗಟ್ಟುವಿಕೆ ಅಂಶವಾಗಿದೆ.4 ವಾರಗಳ ಚಿಕಿತ್ಸೆಯ ನಂತರ, ವಿಷಯದ ವಾರ್ಷಿಕ F8 ಬಳಕೆಯ ದರ ಮತ್ತು ಚಿಕಿತ್ಸೆಯ ಅಗತ್ಯವಿರುವ ABR ಅನ್ನು ಕ್ರಮವಾಗಿ 99% ಮತ್ತು 84% ರಷ್ಟು ಕಡಿಮೆಗೊಳಿಸಲಾಯಿತು, ಮತ್ತು ವ್ಯತ್ಯಾಸವು ಸಂಖ್ಯಾಶಾಸ್ತ್ರೀಯವಾಗಿ ಗಮನಾರ್ಹವಾಗಿದೆ (p<0.001).ಸುರಕ್ಷತಾ ಪ್ರೊಫೈಲ್ ಉತ್ತಮವಾಗಿತ್ತು ಮತ್ತು ಯಾವುದೇ ವಿಷಯದ ಅನುಭವದ F8 ಅಂಶದ ಪ್ರತಿಬಂಧ, ಮಾರಣಾಂತಿಕ ಅಥವಾ ಥ್ರಂಬೋಸಿಸ್ ಅಡ್ಡಪರಿಣಾಮಗಳು ಮತ್ತು ಯಾವುದೇ ಚಿಕಿತ್ಸೆ-ಸಂಬಂಧಿತ ಗಂಭೀರ ಪ್ರತಿಕೂಲ ಘಟನೆಗಳು (SAEs) ವರದಿಯಾಗಿಲ್ಲ.
(11) ಹೆಮ್ಜೆನಿಕ್ಸ್
ಕಂಪನಿ: ಯುನಿಕ್ಯೂರ್ ಕಾರ್ಪೊರೇಷನ್ ಅಭಿವೃದ್ಧಿಪಡಿಸಿದೆ.
ಮಾರುಕಟ್ಟೆಗೆ ಸಮಯ: ನವೆಂಬರ್ 2022 ರಲ್ಲಿ ಮಾರ್ಕೆಟಿಂಗ್ಗಾಗಿ FDA ಯಿಂದ ಅನುಮೋದಿಸಲಾಗಿದೆ.
ಸೂಚನೆಗಳು: ಹಿಮೋಫಿಲಿಯಾ ಬಿ ಹೊಂದಿರುವ ವಯಸ್ಕ ರೋಗಿಗಳ ಚಿಕಿತ್ಸೆಗಾಗಿ.
ಟೀಕೆಗಳು: ಹೆಮ್ಜೆನಿಕ್ಸ್ AAV5 ವೆಕ್ಟರ್ ಅನ್ನು ಆಧರಿಸಿದ ಜೀನ್ ಚಿಕಿತ್ಸೆಯಾಗಿದೆ.ಔಷಧವು ಹೆಪ್ಪುಗಟ್ಟುವಿಕೆ ಅಂಶ IX (FIX) ಜೀನ್ ರೂಪಾಂತರ FIX-ಪಡುವಾದೊಂದಿಗೆ ಸಜ್ಜುಗೊಂಡಿದೆ, ಇದನ್ನು ಅಭಿದಮನಿ ಮೂಲಕ ನಿರ್ವಹಿಸಲಾಗುತ್ತದೆ.ಆಡಳಿತದ ನಂತರ, ಜೀನ್ ಯಕೃತ್ತಿನಲ್ಲಿ FIX ಹೆಪ್ಪುಗಟ್ಟುವಿಕೆ ಅಂಶವನ್ನು ವ್ಯಕ್ತಪಡಿಸಬಹುದು ಮತ್ತು ರಕ್ತವನ್ನು ಪ್ರವೇಶಿಸಿದ ನಂತರ ಹೆಪ್ಪುಗಟ್ಟುವಿಕೆ ಕಾರ್ಯವನ್ನು ನಿರ್ವಹಿಸಲು ಸ್ರವಿಸುತ್ತದೆ, ಆದ್ದರಿಂದ ಚಿಕಿತ್ಸೆಯ ಉದ್ದೇಶವನ್ನು ಸಾಧಿಸಲು, ಸೈದ್ಧಾಂತಿಕವಾಗಿ, ಒಂದು ಆಡಳಿತವು ದೀರ್ಘಕಾಲದವರೆಗೆ ಪರಿಣಾಮಕಾರಿಯಾಗಿದೆ.
(12) ಅಡ್ಸ್ಟಿಲಾಡ್ರಿನ್
ಕಂಪನಿ: ಫೆರಿಂಗ್ ಫಾರ್ಮಾಸ್ಯುಟಿಕಲ್ಸ್ ಅಭಿವೃದ್ಧಿಪಡಿಸಿದೆ.
ಮಾರುಕಟ್ಟೆಗೆ ಸಮಯ: ಡಿಸೆಂಬರ್ 2022 ರಲ್ಲಿ ಮಾರ್ಕೆಟಿಂಗ್ಗಾಗಿ FDA ಯಿಂದ ಅನುಮೋದಿಸಲಾಗಿದೆ.
ಸೂಚನೆಗಳು: ಬ್ಯಾಸಿಲಸ್ ಕ್ಯಾಲ್ಮೆಟ್-ಗ್ಯುರಿನ್ (BCG) ಗೆ ಪ್ರತಿಕ್ರಿಯಿಸದ ಹೆಚ್ಚಿನ ಅಪಾಯದ ಸ್ನಾಯು-ಆಕ್ರಮಣಕಾರಿ ಮೂತ್ರಕೋಶದ ಕ್ಯಾನ್ಸರ್ (NMIBC) ಚಿಕಿತ್ಸೆಗಾಗಿ.
ಟೀಕೆಗಳು: ಆಡ್ಸ್ಟಿಲಾಡ್ರಿನ್ ಒಂದು ಜೀನ್ ಥೆರಪಿಯಾಗಿದ್ದು, ನಕಲು ಮಾಡದ ಅಡೆನೊವೈರಲ್ ವೆಕ್ಟರ್ ಅನ್ನು ಆಧರಿಸಿದೆ, ಇದು ಗುರಿ ಕೋಶಗಳಲ್ಲಿ ಇಂಟರ್ಫೆರಾನ್ ಆಲ್ಫಾ -2 ಬಿ ಪ್ರೋಟೀನ್ ಅನ್ನು ಅತಿಯಾಗಿ ವ್ಯಕ್ತಪಡಿಸುತ್ತದೆ ಮತ್ತು ಮೂತ್ರದ ಕ್ಯಾತಿಟರ್ ಮೂಲಕ ಗಾಳಿಗುಳ್ಳೆಯೊಳಗೆ ನೀಡಲಾಗುತ್ತದೆ (ಪ್ರತಿ ಮೂರು ತಿಂಗಳಿಗೊಮ್ಮೆ ನೀಡಲಾಗುತ್ತದೆ), ವೈರಸ್ ವೆಕ್ಟರ್ ಪರಿಣಾಮಕಾರಿಯಾಗಿ ಪರಿಣಾಮ ಬೀರಬಹುದು. ಒಂದು ಚಿಕಿತ್ಸಕ ಪರಿಣಾಮ.ಈ ಕಾದಂಬರಿ ಜೀನ್ ಥೆರಪಿ ವಿಧಾನವು ರೋಗಿಯ ಸ್ವಂತ ಮೂತ್ರಕೋಶದ ಗೋಡೆಯ ಕೋಶಗಳನ್ನು ಇಂಟರ್ಫೆರಾನ್ ಅನ್ನು ಉತ್ಪಾದಿಸುವ ಚಿಕಣಿ "ಕಾರ್ಖಾನೆ" ಆಗಿ ಪರಿವರ್ತಿಸುತ್ತದೆ, ಇದರಿಂದಾಗಿ ಕ್ಯಾನ್ಸರ್ ವಿರುದ್ಧ ಹೋರಾಡುವ ರೋಗಿಯ ಸಾಮರ್ಥ್ಯವನ್ನು ಹೆಚ್ಚಿಸುತ್ತದೆ.
ಹೆಚ್ಚಿನ ಅಪಾಯದ BCG-ಪ್ರತಿಕ್ರಿಯಿಸದ NMIBC ಹೊಂದಿರುವ 157 ರೋಗಿಗಳನ್ನು ಒಳಗೊಂಡಂತೆ ಮಲ್ಟಿಸೆಂಟರ್ ಕ್ಲಿನಿಕಲ್ ಅಧ್ಯಯನದಲ್ಲಿ Adstiladrin ನ ಸುರಕ್ಷತೆ ಮತ್ತು ಪರಿಣಾಮಕಾರಿತ್ವವನ್ನು ಮೌಲ್ಯಮಾಪನ ಮಾಡಲಾಗಿದೆ.ರೋಗಿಗಳು ಪ್ರತಿ ಮೂರು ತಿಂಗಳಿಗೊಮ್ಮೆ 12 ತಿಂಗಳವರೆಗೆ ಅಥವಾ ಉನ್ನತ ದರ್ಜೆಯ NMIBC ಯ ಚಿಕಿತ್ಸೆ ಅಥವಾ ಮರುಕಳಿಸುವಿಕೆಗೆ ಸ್ವೀಕಾರಾರ್ಹವಲ್ಲದ ವಿಷತ್ವವನ್ನು ಪಡೆಯುವವರೆಗೆ ಅಡ್ಸ್ಟಿಲಾಡ್ರಿನ್ ಅನ್ನು ಪಡೆದರು.ಒಟ್ಟಾರೆಯಾಗಿ, ಅಡ್ಸ್ಟಿಲಾಡ್ರಿನ್ನೊಂದಿಗೆ ಚಿಕಿತ್ಸೆ ಪಡೆದ ದಾಖಲಾದ 51 ಪ್ರತಿಶತ ರೋಗಿಗಳು ಸಂಪೂರ್ಣ ಪ್ರತಿಕ್ರಿಯೆಯನ್ನು ಸಾಧಿಸಿದ್ದಾರೆ (ಸಿಸ್ಟೊಸ್ಕೋಪಿ, ಬಯಾಪ್ಸಿ ಅಂಗಾಂಶ ಮತ್ತು ಮೂತ್ರದಲ್ಲಿ ಕಂಡುಬರುವ ಕ್ಯಾನ್ಸರ್ನ ಎಲ್ಲಾ ಚಿಹ್ನೆಗಳ ಕಣ್ಮರೆಯಾಗುವುದು).
3. ಸಣ್ಣ ನ್ಯೂಕ್ಲಿಯಿಕ್ ಆಮ್ಲ ಔಷಧಗಳು
(1) ವಿತ್ರವೇನೆ
ಕಂಪನಿ: ಅಯೋನಿಸ್ ಫಾರ್ಮಾ (ಹಿಂದೆ ಐಸಿಸ್ ಫಾರ್ಮಾ) ಮತ್ತು ನೊವಾರ್ಟಿಸ್ನಿಂದ ಜಂಟಿಯಾಗಿ ಅಭಿವೃದ್ಧಿಪಡಿಸಲಾಗಿದೆ.
ಮಾರುಕಟ್ಟೆಗೆ ಸಮಯ: 1998 ಮತ್ತು 1999 ರಲ್ಲಿ, ಇದನ್ನು FDA ಮತ್ತು EU EMA ನಿಂದ ಮಾರ್ಕೆಟಿಂಗ್ ಮಾಡಲು ಅನುಮೋದಿಸಲಾಯಿತು.
ಸೂಚನೆಗಳು: ಎಚ್ಐವಿ-ಪಾಸಿಟಿವ್ ರೋಗಿಗಳಲ್ಲಿ ಸೈಟೊಮೆಗಾಲೊವೈರಸ್ ರೆಟಿನೈಟಿಸ್ ಚಿಕಿತ್ಸೆಗಾಗಿ.
ಟೀಕೆಗಳು: ವಿಟ್ರಾವೆನ್ ಎಂಬುದು ಆಂಟಿಸೆನ್ಸ್ ಆಲಿಗೋನ್ಯೂಕ್ಲಿಯೋಟೈಡ್ ಔಷಧವಾಗಿದೆ, ಇದು ವಿಶ್ವದಲ್ಲೇ ಮಾರುಕಟ್ಟೆಗೆ ಅನುಮೋದಿಸಲಾದ ಮೊದಲ ಆಲಿಗೋನ್ಯೂಕ್ಲಿಯೋಟೈಡ್ ಔಷಧವಾಗಿದೆ.ಪಟ್ಟಿಯ ಆರಂಭಿಕ ಹಂತದಲ್ಲಿ, CMV ವಿರೋಧಿ ಔಷಧಿಗಳ ಮಾರುಕಟ್ಟೆ ಬೇಡಿಕೆಯು ಬಹಳ ತುರ್ತು;ನಂತರ, ಹೆಚ್ಚು ಸಕ್ರಿಯವಾದ ಆಂಟಿರೆಟ್ರೋವೈರಲ್ ಚಿಕಿತ್ಸೆಯ ಬೆಳವಣಿಗೆಯಿಂದಾಗಿ, CMV ಪ್ರಕರಣಗಳ ಸಂಖ್ಯೆಯು ತೀವ್ರವಾಗಿ ಕುಸಿಯಿತು.ನಿಧಾನಗತಿಯ ಮಾರುಕಟ್ಟೆ ಬೇಡಿಕೆಯಿಂದಾಗಿ, ಔಷಧವನ್ನು 2002 ಮತ್ತು 2006 ರಲ್ಲಿ EU ದೇಶಗಳಲ್ಲಿ ಮತ್ತು ಯುನೈಟೆಡ್ ಸ್ಟೇಟ್ಸ್ನಲ್ಲಿ ಹಿಂತೆಗೆದುಕೊಳ್ಳಲಾಯಿತು.
(2) ಮ್ಯಾಕುಜೆನ್
ಕಂಪನಿ: ಫಿಜರ್ ಮತ್ತು ಐಟೆಕ್ನಿಂದ ಸಹ-ಅಭಿವೃದ್ಧಿಪಡಿಸಲಾಗಿದೆ.
ಮಾರುಕಟ್ಟೆಗೆ ಸಮಯ: 2004 ರಲ್ಲಿ ಯುನೈಟೆಡ್ ಸ್ಟೇಟ್ಸ್ನಲ್ಲಿ ಪಟ್ಟಿ ಮಾಡಲು ಅನುಮೋದಿಸಲಾಗಿದೆ.
ಸೂಚನೆಗಳು: ನಿಯೋವಾಸ್ಕುಲರ್ ವಯಸ್ಸಿಗೆ ಸಂಬಂಧಿಸಿದ ಮ್ಯಾಕ್ಯುಲರ್ ಡಿಜೆನರೇಶನ್ ಚಿಕಿತ್ಸೆಗಾಗಿ.
ಟೀಕೆಗಳು: ಮ್ಯಾಕುಜೆನ್ ಒಂದು ಪೆಜಿಲೇಟೆಡ್ ಮಾರ್ಪಡಿಸಿದ ಆಲಿಗೋನ್ಯೂಕ್ಲಿಯೊಟೈಡ್ ಔಷಧವಾಗಿದೆ, ಇದು ನಾಳೀಯ ಎಂಡೋಥೀಲಿಯಲ್ ಬೆಳವಣಿಗೆಯ ಅಂಶವನ್ನು (VEGF165 ಸಬ್ಟೈಪ್) ಗುರಿಯಾಗಿಸಬಹುದು ಮತ್ತು ಬಂಧಿಸಬಹುದು ಮತ್ತು ಆಡಳಿತದ ವಿಧಾನವು ಇಂಟ್ರಾವಿಟ್ರಿಯಲ್ ಇಂಜೆಕ್ಷನ್ ಆಗಿದೆ.
(3) ಡಿಫಿಟೆಲಿಯೊ
ಕಂಪನಿ: ಜಾಝ್ ಫಾರ್ಮಾಸ್ಯುಟಿಕಲ್ಸ್ ಅಭಿವೃದ್ಧಿಪಡಿಸಿದೆ.
ಮಾರುಕಟ್ಟೆಗೆ ಸಮಯ: ಇದನ್ನು 2013 ರಲ್ಲಿ ಯುರೋಪಿಯನ್ ಯೂನಿಯನ್ ಮಾರ್ಕೆಟಿಂಗ್ಗೆ ಅನುಮೋದಿಸಿತು ಮತ್ತು ಮಾರ್ಚ್ 2016 ರಲ್ಲಿ ಮಾರ್ಕೆಟಿಂಗ್ಗಾಗಿ ಎಫ್ಡಿಎ ಅನುಮೋದಿಸಿತು.
ಸೂಚನೆಗಳು: ಹೆಮಟೊಪಯಟಿಕ್ ಸ್ಟೆಮ್ ಸೆಲ್ ಕಸಿ ನಂತರ ಮೂತ್ರಪಿಂಡ ಅಥವಾ ಶ್ವಾಸಕೋಶದ ಅಪಸಾಮಾನ್ಯ ಕ್ರಿಯೆಗೆ ಸಂಬಂಧಿಸಿದ ಹೆಪಾಟಿಕ್ ವೆನೊ-ಆಕ್ಲೂಸಿವ್ ಕಾಯಿಲೆಯ ಚಿಕಿತ್ಸೆಗಾಗಿ.
ಟೀಕೆಗಳು: ಡಿಫಿಟೆಲಿಯೊ ಒಲಿಗೋನ್ಯೂಕ್ಲಿಯೊಟೈಡ್ ಔಷಧವಾಗಿದೆ, ಇದು ಪ್ಲಾಸ್ಮಿನ್ ಗುಣಲಕ್ಷಣಗಳೊಂದಿಗೆ ಆಲಿಗೋನ್ಯೂಕ್ಲಿಯೋಟೈಡ್ಗಳ ಮಿಶ್ರಣವಾಗಿದೆ.ವಾಣಿಜ್ಯ ಕಾರಣಗಳಿಗಾಗಿ 2009 ರಲ್ಲಿ ಮಾರುಕಟ್ಟೆಯಿಂದ ಹಿಂತೆಗೆದುಕೊಳ್ಳಲಾಯಿತು.
(4) ಕೈಮ್ರೊ
ಕಂಪನಿ: ಅಯೋನಿಸ್ ಫಾರ್ಮಾ ಮತ್ತು ಕ್ಯಾಸ್ಟಲ್ನಿಂದ ಸಹ-ಅಭಿವೃದ್ಧಿಪಡಿಸಲಾಗಿದೆ.
ಮಾರುಕಟ್ಟೆಗೆ ಸಮಯ: 2013 ರಲ್ಲಿ, ಯುನೈಟೆಡ್ ಸ್ಟೇಟ್ಸ್ನಲ್ಲಿ ಅನಾಥ ಔಷಧವಾಗಿ ಮಾರ್ಕೆಟಿಂಗ್ ಮಾಡಲು ಅನುಮೋದಿಸಲಾಯಿತು.
ಸೂಚನೆಗಳು: ಹೋಮೋಜೈಗಸ್ ಕೌಟುಂಬಿಕ ಹೈಪರ್ಕೊಲೆಸ್ಟರಾಲ್ಮಿಯಾದ ಸಹಾಯಕ ಚಿಕಿತ್ಸೆಗಾಗಿ.
ಟೀಕೆಗಳು: ಕೈನಾಮ್ರೊ ಒಂದು ಆಂಟಿಸೆನ್ಸ್ ಆಲಿಗೊನ್ಯೂಕ್ಲಿಯೊಟೈಡ್ ಔಷಧವಾಗಿದೆ, ಇದು ಮಾನವನ ಅಪೊ B-100 mRNA ಯನ್ನು ಗುರಿಯಾಗಿಸುವ ಆಂಟಿಸೆನ್ಸ್ ಆಲಿಗೋನ್ಯೂಕ್ಲಿಯೊಟೈಡ್ ಆಗಿದೆ.ವಾರಕ್ಕೊಮ್ಮೆ ಕೈನಾಮ್ರೊವನ್ನು 200 ಮಿಗ್ರಾಂ ಸಬ್ಕ್ಯುಟೇನಿಯಸ್ ಆಗಿ ನೀಡಲಾಗುತ್ತದೆ.
(5) ಸ್ಪಿನ್ರಾಜಾ
ಕಂಪನಿ: ಅಯೋನಿಸ್ ಫಾರ್ಮಾಸ್ಯುಟಿಕಲ್ಸ್ ಅಭಿವೃದ್ಧಿಪಡಿಸಿದೆ.
ಮಾರುಕಟ್ಟೆಗೆ ಸಮಯ: ಡಿಸೆಂಬರ್ 2016 ರಲ್ಲಿ ಮಾರ್ಕೆಟಿಂಗ್ಗಾಗಿ FDA ಯಿಂದ ಅನುಮೋದಿಸಲಾಗಿದೆ.
ಸೂಚನೆಗಳು: ಬೆನ್ನುಮೂಳೆಯ ಸ್ನಾಯು ಕ್ಷೀಣತೆ (SMA) ಚಿಕಿತ್ಸೆಗಾಗಿ.
ಟೀಕೆಗಳು: ಸ್ಪಿನ್ರಾಜಾ (ನುಸಿನರ್ಸೆನ್) ಒಂದು ಆಂಟಿಸೆನ್ಸ್ ಆಲಿಗೋನ್ಯೂಕ್ಲಿಯೊಟೈಡ್ ಔಷಧವಾಗಿದೆ.SMN2 ಎಕ್ಸಾನ್ 7 ರ ಸೀಳಿನ ಸೈಟ್ಗೆ ಬಂಧಿಸುವ ಮೂಲಕ, ಸ್ಪಿನ್ರಾಜಾ SMN2 ಜೀನ್ನ RNA ಸೀಳನ್ನು ಬದಲಾಯಿಸಬಹುದು, ಇದರಿಂದಾಗಿ ಸಂಪೂರ್ಣ ಕ್ರಿಯಾತ್ಮಕ SMN ಪ್ರೊಟೀನ್ ಉತ್ಪಾದನೆಯನ್ನು ಹೆಚ್ಚಿಸುತ್ತದೆ.ಆಗಸ್ಟ್ 2016 ರಲ್ಲಿ, ಸ್ಪಿನ್ರಾಜಾಗೆ ಜಾಗತಿಕ ಹಕ್ಕುಗಳನ್ನು ಪಡೆಯಲು BIOGEN ತನ್ನ ಆಯ್ಕೆಯನ್ನು ಚಲಾಯಿಸಿತು.Spinraza ಕೇವಲ 2011 ರಲ್ಲಿ ಮಾನವರಲ್ಲಿ ತನ್ನ ಮೊದಲ ಕ್ಲಿನಿಕಲ್ ಪ್ರಯೋಗವನ್ನು ಪ್ರಾರಂಭಿಸಿತು. ಕೇವಲ 5 ವರ್ಷಗಳಲ್ಲಿ, FDA ಯಿಂದ 2016 ರಲ್ಲಿ ಮಾರ್ಕೆಟಿಂಗ್ ಮಾಡಲು ಅನುಮೋದಿಸಲಾಯಿತು, ಇದು FDA ಯ ಸಂಪೂರ್ಣ ಮನ್ನಣೆಯನ್ನು ಅದರ ಪರಿಣಾಮಕಾರಿತ್ವವನ್ನು ಪ್ರತಿಬಿಂಬಿಸುತ್ತದೆ.ಏಪ್ರಿಲ್ 2019 ರಲ್ಲಿ ಚೀನಾದಲ್ಲಿ ಮಾರ್ಕೆಟಿಂಗ್ ಮಾಡಲು ಔಷಧವನ್ನು ಅನುಮೋದಿಸಲಾಗಿದೆ. ಚೀನಾದಲ್ಲಿ ಸ್ಪಿನ್ರಾಜಾಗೆ ಸಂಪೂರ್ಣ ಅನುಮೋದನೆ ಚಕ್ರವು 6 ತಿಂಗಳಿಗಿಂತ ಕಡಿಮೆಯಿತ್ತು ಮತ್ತು ಸ್ಪಿನ್ರಾಜಾವನ್ನು ಯುನೈಟೆಡ್ ಸ್ಟೇಟ್ಸ್ನಲ್ಲಿ ಮೊದಲು ಅನುಮೋದಿಸಿ 2 ವರ್ಷಗಳು ಮತ್ತು 2 ತಿಂಗಳುಗಳು.ಚೀನಾದಲ್ಲಿ ಪಟ್ಟಿ ಮಾಡುವ ವೇಗವು ಈಗಾಗಲೇ ತುಂಬಾ ವೇಗವಾಗಿದೆ.ಔಷಧಿ ಮೌಲ್ಯಮಾಪನ ಕೇಂದ್ರವು ನವೆಂಬರ್ 1, 2018 ರಂದು "ಕ್ಲಿನಿಕಲ್ ಅಭ್ಯಾಸದಲ್ಲಿ ತುರ್ತಾಗಿ ಅಗತ್ಯವಿರುವ ಸಾಗರೋತ್ತರ ಹೊಸ ಔಷಧಿಗಳ ಮೊದಲ ಬ್ಯಾಚ್ನ ಪಟ್ಟಿಯನ್ನು ಪ್ರಕಟಿಸುವ ಕುರಿತು ಸೂಚನೆಯನ್ನು" ಬಿಡುಗಡೆ ಮಾಡಿದೆ ಮತ್ತು ವೇಗವರ್ಧಿತ ಪರಿಶೀಲನೆಗಾಗಿ 40 ವಿದೇಶಿ ಹೊಸ drugs ಷಧಿಗಳ ಮೊದಲ ಬ್ಯಾಚ್ನಲ್ಲಿ ಸೇರಿಸಲ್ಪಟ್ಟಿದೆ.
(6) ಎಕ್ಸಾಂಡಿಸ್ 51
ಕಂಪನಿ: AVI ಬಯೋಫಾರ್ಮಾದಿಂದ ಅಭಿವೃದ್ಧಿಪಡಿಸಲಾಗಿದೆ (ನಂತರ ಇದನ್ನು ಸರೆಪ್ಟಾ ಥೆರಪ್ಯೂಟಿಕ್ಸ್ ಎಂದು ಮರುನಾಮಕರಣ ಮಾಡಲಾಯಿತು).
ಮಾರುಕಟ್ಟೆಗೆ ಸಮಯ: ಸೆಪ್ಟೆಂಬರ್ 2016 ರಲ್ಲಿ, ಇದನ್ನು FDA ಯಿಂದ ಮಾರ್ಕೆಟಿಂಗ್ ಮಾಡಲು ಅನುಮೋದಿಸಲಾಗಿದೆ.
ಸೂಚನೆಗಳು: ಡಿಎಮ್ಡಿ ಜೀನ್ನಲ್ಲಿ ಎಕ್ಸಾನ್ 51 ಸ್ಕಿಪ್ಪಿಂಗ್ ಜೀನ್ ರೂಪಾಂತರದೊಂದಿಗೆ ಡುಚೆನ್ ಮಸ್ಕ್ಯುಲರ್ ಡಿಸ್ಟ್ರೋಫಿ (ಡಿಎಮ್ಡಿ) ಚಿಕಿತ್ಸೆಗಾಗಿ.
ಟೀಕೆಗಳು: ಎಕ್ಸಾಂಡಿಸ್ 51 ಒಂದು ಆಂಟಿಸೆನ್ಸ್ ಆಲಿಗೊನ್ಯೂಕ್ಲಿಯೊಟೈಡ್ ಔಷಧವಾಗಿದೆ, ಆಂಟಿಸೆನ್ಸ್ ಆಲಿಗೊನ್ಯೂಕ್ಲಿಯೊಟೈಡ್ ಡಿಎಮ್ಡಿ ಜೀನ್ನ ಪೂರ್ವ-ಎಂಆರ್ಎನ್ಎಯ ಎಕ್ಸಾನ್ 51 ರ ಸ್ಥಾನಕ್ಕೆ ಬಂಧಿಸುತ್ತದೆ, ಇದರ ಪರಿಣಾಮವಾಗಿ ಪ್ರಬುದ್ಧ ಎಮ್ಆರ್ಎನ್ಎ ರಚನೆಯಾಗುತ್ತದೆ, ಎಕ್ಸಾನ್ 51 ರ ಭಾಗವು ಎಕ್ಸೈಶನ್ ಅನ್ನು ನಿರ್ಬಂಧಿಸುತ್ತದೆ, ಆ ಮೂಲಕ ಎಮ್ಆರ್ಎನ್ಎ ಓದುವಿಕೆಯನ್ನು ರೂಪಿಸಲು ಭಾಗಶಃ ಸಂಶ್ಲೇಷಿಸಲು ಸಹಾಯ ಮಾಡುತ್ತದೆ. ಸಾಮಾನ್ಯ ಪ್ರೋಟೀನ್ಗಿಂತ, ಇದರಿಂದಾಗಿ ರೋಗಿಯ ರೋಗಲಕ್ಷಣಗಳನ್ನು ಸುಧಾರಿಸುತ್ತದೆ.
(7) ತೆಗ್ಸೇಡಿ
ಕಂಪನಿ: ಅಯೋನಿಸ್ ಫಾರ್ಮಾಸ್ಯುಟಿಕಲ್ಸ್ ಅಭಿವೃದ್ಧಿಪಡಿಸಿದೆ.
ಮಾರುಕಟ್ಟೆಗೆ ಸಮಯ: ಜುಲೈ 2018 ರಲ್ಲಿ ಯುರೋಪಿಯನ್ ಯೂನಿಯನ್ ಇದನ್ನು ಮಾರ್ಕೆಟಿಂಗ್ ಮಾಡಲು ಅನುಮೋದಿಸಿದೆ.
ಸೂಚನೆಗಳು: ಆನುವಂಶಿಕ ಟ್ರಾನ್ಸ್ಥೈರೆಟಿನ್ ಅಮಿಲೋಯ್ಡೋಸಿಸ್ (hATTR) ಚಿಕಿತ್ಸೆಗಾಗಿ.
ಟೀಕೆಗಳು: ಟೆಗ್ಸೆಡಿ ಎಂಬುದು ಟ್ರಾನ್ಸ್ಥೈರೆಟಿನ್ ಎಮ್ಆರ್ಎನ್ಎ ಗುರಿಯಾಗಿಸುವ ಆಂಟಿಸೆನ್ಸ್ ಆಲಿಗೋನ್ಯೂಕ್ಲಿಯೊಟೈಡ್ ಔಷಧವಾಗಿದೆ.ಇದು hATTR ಚಿಕಿತ್ಸೆಗಾಗಿ ವಿಶ್ವದಲ್ಲೇ ಅನುಮೋದಿಸಲಾದ ಮೊದಲ ಔಷಧವಾಗಿದೆ.ಇದನ್ನು ಸಬ್ಕ್ಯುಟೇನಿಯಸ್ ಇಂಜೆಕ್ಷನ್ ಮೂಲಕ ನಿರ್ವಹಿಸಲಾಗುತ್ತದೆ.ಔಷಧವು ಟ್ರಾನ್ಸ್ಥೈರೆಟಿನ್ (ATTR) ನ mRNA ಯನ್ನು ಗುರಿಯಾಗಿಟ್ಟುಕೊಂಡು ATTR ಪ್ರೊಟೀನ್ನ ಉತ್ಪಾದನೆಯನ್ನು ಕಡಿಮೆ ಮಾಡುತ್ತದೆ ಮತ್ತು ATTR ಚಿಕಿತ್ಸೆಯಲ್ಲಿ ಉತ್ತಮ ಲಾಭ-ಅಪಾಯದ ಅನುಪಾತವನ್ನು ಹೊಂದಿದೆ ಮತ್ತು ರೋಗಿಯ ನರರೋಗ ಮತ್ತು ಜೀವನದ ಗುಣಮಟ್ಟವನ್ನು ಗಣನೀಯವಾಗಿ ಸುಧಾರಿಸಲಾಗಿದೆ ಮತ್ತು ಇದು TTR ರೂಪಾಂತರದ ಪ್ರಕಾರಗಳೊಂದಿಗೆ ಹೊಂದಿಕೊಳ್ಳುತ್ತದೆ, ರೋಗದ ಹಂತ ಅಥವಾ ಕಾರ್ಡಿಯೊಮಿಯೊಪತಿಯ ಉಪಸ್ಥಿತಿಯು ಸಂಬಂಧಿಸಿಲ್ಲ.
(8) ಆನ್ಪಾಟ್ರೊ
ಕಂಪನಿ: ಅಲ್ನಿಲಾಮ್ ಕಾರ್ಪೊರೇಷನ್ ಮತ್ತು ಸನೋಫಿ ಕಾರ್ಪೊರೇಷನ್ ಜಂಟಿಯಾಗಿ ಅಭಿವೃದ್ಧಿಪಡಿಸಿದೆ.
ಮಾರುಕಟ್ಟೆಗೆ ಸಮಯ: 2018 ರಲ್ಲಿ ಯುನೈಟೆಡ್ ಸ್ಟೇಟ್ಸ್ನಲ್ಲಿ ಪಟ್ಟಿ ಮಾಡಲು ಅನುಮೋದಿಸಲಾಗಿದೆ.
ಸೂಚನೆಗಳು: ಆನುವಂಶಿಕ ಟ್ರಾನ್ಸ್ಥೈರೆಟಿನ್ ಅಮಿಲೋಯ್ಡೋಸಿಸ್ (hATTR) ಚಿಕಿತ್ಸೆಗಾಗಿ.
ಟೀಕೆಗಳು: ಆನ್ಪಾಟ್ರೊ ಎಂಬುದು ಟ್ರಾನ್ಸ್ಥೈರೆಟಿನ್ ಎಮ್ಆರ್ಎನ್ಎ ಗುರಿಯಾಗಿಸುವ ಒಂದು ಸಿಆರ್ಎನ್ಎ ಔಷಧವಾಗಿದ್ದು, ಇದು ಯಕೃತ್ತಿನಲ್ಲಿ ಎಟಿಟಿಆರ್ ಪ್ರೊಟೀನ್ ಉತ್ಪಾದನೆಯನ್ನು ಕಡಿಮೆ ಮಾಡುತ್ತದೆ ಮತ್ತು ಟ್ರಾನ್ಸ್ಥೈರೆಟಿನ್ (ಎಟಿಟಿಆರ್) ನ ಎಮ್ಆರ್ಎನ್ಎಯನ್ನು ಗುರಿಯಾಗಿಸಿಕೊಂಡು ಬಾಹ್ಯ ನರಗಳಲ್ಲಿ ಅಮಿಲಾಯ್ಡ್ ನಿಕ್ಷೇಪಗಳ ಸಂಗ್ರಹವನ್ನು ಕಡಿಮೆ ಮಾಡುತ್ತದೆ, ಇದರಿಂದಾಗಿ ರೋಗದ ಲಕ್ಷಣಗಳನ್ನು ಸುಧಾರಿಸುತ್ತದೆ ಮತ್ತು ನಿವಾರಿಸುತ್ತದೆ.
(9) ಗಿವ್ಲಾರಿ
ಕಂಪನಿ: ಅಲ್ನಿಲಾಮ್ ಕಾರ್ಪೊರೇಷನ್ ಅಭಿವೃದ್ಧಿಪಡಿಸಿದೆ.
ಮಾರುಕಟ್ಟೆಗೆ ಸಮಯ: ನವೆಂಬರ್ 2019 ರಲ್ಲಿ ಮಾರ್ಕೆಟಿಂಗ್ಗಾಗಿ FDA ಯಿಂದ ಅನುಮೋದಿಸಲಾಗಿದೆ.
ಸೂಚನೆಗಳು: ವಯಸ್ಕರಲ್ಲಿ ತೀವ್ರವಾದ ಹೆಪಾಟಿಕ್ ಪೋರ್ಫೈರಿಯಾ (AHP) ಚಿಕಿತ್ಸೆಗಾಗಿ.
ಟಿಪ್ಪಣಿಗಳು: ಗಿವ್ಲಾರಿ ಒಂದು siRNA ಔಷಧವಾಗಿದೆ, ಇದು Onpattro ನಂತರ ಮಾರುಕಟ್ಟೆಗೆ ಅನುಮೋದಿಸಲಾದ ಎರಡನೇ siRNA ಔಷಧವಾಗಿದೆ.ಆಡಳಿತದ ವಿಧಾನವೆಂದರೆ ಸಬ್ಕ್ಯುಟೇನಿಯಸ್ ಇಂಜೆಕ್ಷನ್.ಔಷಧವು ALAS1 ಪ್ರೋಟೀನ್ನ mRNA ಯನ್ನು ಗುರಿಯಾಗಿಸುತ್ತದೆ ಮತ್ತು Givlaari ಯೊಂದಿಗಿನ ಮಾಸಿಕ ಚಿಕಿತ್ಸೆಯು ಯಕೃತ್ತಿನಲ್ಲಿ ALAS1 ಮಟ್ಟವನ್ನು ಗಣನೀಯವಾಗಿ ಮತ್ತು ಶಾಶ್ವತವಾಗಿ ಕಡಿಮೆ ಮಾಡುತ್ತದೆ, ಇದರಿಂದಾಗಿ ನ್ಯೂರೋಟಾಕ್ಸಿಕ್ ALA ಮತ್ತು PBG ಮಟ್ಟವನ್ನು ಸಾಮಾನ್ಯ ಮಟ್ಟಕ್ಕೆ ತಗ್ಗಿಸುತ್ತದೆ, ಇದರಿಂದಾಗಿ ರೋಗಿಯ ರೋಗದ ಲಕ್ಷಣಗಳನ್ನು ನಿವಾರಿಸುತ್ತದೆ.ಪ್ಲೇಸ್ಬೊ ಗುಂಪಿಗೆ ಹೋಲಿಸಿದರೆ ಗಿವ್ಲಾರಿಯೊಂದಿಗೆ ಚಿಕಿತ್ಸೆ ಪಡೆದ ರೋಗಿಗಳು ರೋಗಗ್ರಸ್ತವಾಗುವಿಕೆಗಳ ಸಂಖ್ಯೆಯಲ್ಲಿ 74% ಕಡಿತವನ್ನು ಹೊಂದಿದ್ದಾರೆ ಎಂದು ಡೇಟಾ ತೋರಿಸಿದೆ.
(10) Vyondys53
ಕಂಪನಿ: ಸರೆಪ್ಟಾ ಥೆರಪ್ಯೂಟಿಕ್ಸ್ನಿಂದ ಅಭಿವೃದ್ಧಿಪಡಿಸಲಾಗಿದೆ.
ಮಾರುಕಟ್ಟೆಗೆ ಸಮಯ: ಡಿಸೆಂಬರ್ 2019 ರಲ್ಲಿ ಮಾರ್ಕೆಟಿಂಗ್ಗಾಗಿ FDA ಯಿಂದ ಅನುಮೋದಿಸಲಾಗಿದೆ.
ಸೂಚನೆಗಳು: ಡಿಸ್ಟ್ರೋಫಿನ್ ಜೀನ್ ಎಕ್ಸಾನ್ 53 ಸ್ಪ್ಲೈಸಿಂಗ್ ಮ್ಯುಟೇಶನ್ ಹೊಂದಿರುವ DMD ರೋಗಿಗಳ ಚಿಕಿತ್ಸೆಗಾಗಿ.
ಟೀಕೆಗಳು: Vyondys 53 ಒಂದು ಆಂಟಿಸೆನ್ಸ್ ಆಲಿಗೋನ್ಯೂಕ್ಲಿಯೋಟೈಡ್ ಔಷಧವಾಗಿದೆ, ಇದು ಡಿಸ್ಟ್ರೋಫಿನ್ ಪೂರ್ವ-mRNA ಯ ಸ್ಪ್ಲೈಸಿಂಗ್ ಪ್ರಕ್ರಿಯೆಯನ್ನು ಗುರಿಯಾಗಿಸುತ್ತದೆ.ಎಕ್ಸಾನ್ 53 ಭಾಗಶಃ ಮೊಟಕುಗೊಂಡಿದೆ, ಅಂದರೆ ಪ್ರಬುದ್ಧ mRNA ಯಲ್ಲಿ ಇರುವುದಿಲ್ಲ, ಮತ್ತು ಮೊಟಕುಗೊಳಿಸಿದ ಆದರೆ ಇನ್ನೂ ಕಾರ್ಯನಿರ್ವಹಿಸುವ ಡಿಸ್ಟ್ರೋಫಿನ್ ಅನ್ನು ಉತ್ಪಾದಿಸಲು ವಿನ್ಯಾಸಗೊಳಿಸಲಾಗಿದೆ, ಇದರಿಂದಾಗಿ ರೋಗಿಗಳಲ್ಲಿ ವ್ಯಾಯಾಮ ಸಾಮರ್ಥ್ಯವನ್ನು ಸುಧಾರಿಸುತ್ತದೆ.
(11) ವೇಲಿವ್ರಾ
ಕಂಪನಿ: ಅಯೋನಿಸ್ ಫಾರ್ಮಾಸ್ಯುಟಿಕಲ್ಸ್ ಮತ್ತು ಅದರ ಅಂಗಸಂಸ್ಥೆ Akcea ಥೆರಪ್ಯೂಟಿಕ್ಸ್ ಅಭಿವೃದ್ಧಿಪಡಿಸಿದೆ.
ಮಾರುಕಟ್ಟೆಗೆ ಸಮಯ: ಮೇ 2019 ರಲ್ಲಿ ಯುರೋಪಿಯನ್ ಮೆಡಿಸಿನ್ಸ್ ಏಜೆನ್ಸಿ (ಇಎಂಎ) ಇದನ್ನು ಮಾರ್ಕೆಟಿಂಗ್ ಮಾಡಲು ಅನುಮೋದಿಸಿದೆ.
ಸೂಚನೆಗಳು: ಕೌಟುಂಬಿಕ ಕೈಲೋಮೈಕ್ರೊನೆಮಿಯಾ ಸಿಂಡ್ರೋಮ್ (ಎಫ್ಸಿಎಸ್) ಹೊಂದಿರುವ ವಯಸ್ಕ ರೋಗಿಗಳಲ್ಲಿ ಆಹಾರ ನಿಯಂತ್ರಣದ ಜೊತೆಗೆ ಸಹಾಯಕ ಚಿಕಿತ್ಸೆಯಾಗಿ.
ಟೀಕೆಗಳು: Waylivra ಒಂದು ಆಂಟಿಸೆನ್ಸ್ ಆಲಿಗೋನ್ಯೂಕ್ಲಿಯೊಟೈಡ್ ಔಷಧವಾಗಿದೆ, ಇದು FCS ಚಿಕಿತ್ಸೆಗಾಗಿ ವಿಶ್ವದಲ್ಲಿ ಮಾರುಕಟ್ಟೆಗೆ ಅನುಮೋದಿಸಲಾದ ಮೊದಲ ಔಷಧವಾಗಿದೆ.
(12) ಲೆಕ್ವಿಯೊ
ಕಂಪನಿ: ನೊವಾರ್ಟಿಸ್ನಿಂದ ಅಭಿವೃದ್ಧಿಪಡಿಸಲಾಗಿದೆ.
ಮಾರುಕಟ್ಟೆಗೆ ಸಮಯ: ಡಿಸೆಂಬರ್ 2020 ರಲ್ಲಿ ಮಾರ್ಕೆಟಿಂಗ್ಗಾಗಿ ಯುರೋಪಿಯನ್ ಒಕ್ಕೂಟದಿಂದ ಅನುಮೋದಿಸಲಾಗಿದೆ.
ಸೂಚನೆಗಳು: ಪ್ರಾಥಮಿಕ ಹೈಪರ್ಕೊಲೆಸ್ಟರಾಲ್ಮಿಯಾ (ಹೆಟೆರೊಜೈಗಸ್ ಫ್ಯಾಮಿಲಿಯಲ್ ಮತ್ತು ನಾನ್-ಫ್ಯಾಮಿಲಿಯಲ್) ಅಥವಾ ಮಿಶ್ರ ಡಿಸ್ಲಿಪಿಡೆಮಿಯಾ ಹೊಂದಿರುವ ವಯಸ್ಕರ ಚಿಕಿತ್ಸೆಗಾಗಿ.
ಟೀಕೆಗಳು: Leqvio PCSK9 mRNA ಅನ್ನು ಗುರಿಯಾಗಿಸುವ siRNA ಔಷಧವಾಗಿದೆ.ಇದು ಕೊಲೆಸ್ಟ್ರಾಲ್ (LDL-C) ಅನ್ನು ಕಡಿಮೆ ಮಾಡಲು ವಿಶ್ವದ ಮೊದಲ siRNA ಚಿಕಿತ್ಸೆಯಾಗಿದೆ.ಇದನ್ನು ಸಬ್ಕ್ಯುಟೇನಿಯಸ್ ಇಂಜೆಕ್ಷನ್ ಮೂಲಕ ನಿರ್ವಹಿಸಲಾಗುತ್ತದೆ.ಔಷಧವು ಆರ್ಎನ್ಎ ಹಸ್ತಕ್ಷೇಪದ ಮೂಲಕ PCSK9 ಪ್ರೊಟೀನ್ ಮಟ್ಟವನ್ನು ಕಡಿಮೆ ಮಾಡುತ್ತದೆ, ಇದರಿಂದಾಗಿ LDL-C ಮಟ್ಟವನ್ನು ಕಡಿಮೆ ಮಾಡುತ್ತದೆ.ಸ್ಟ್ಯಾಟಿನ್ಗಳ ಗರಿಷ್ಠ ಸಹಿಷ್ಣು ಡೋಸ್ನೊಂದಿಗೆ ಚಿಕಿತ್ಸೆಯ ನಂತರ LDL-C ಮಟ್ಟವನ್ನು ಗುರಿಯ ಮಟ್ಟಕ್ಕೆ ಇಳಿಸಲು ಸಾಧ್ಯವಾಗದ ರೋಗಿಗಳಿಗೆ, Leqvio LDL-C ಅನ್ನು ಸುಮಾರು 50% ರಷ್ಟು ಕಡಿಮೆ ಮಾಡಬಹುದು ಎಂದು ಕ್ಲಿನಿಕಲ್ ಡೇಟಾ ತೋರಿಸುತ್ತದೆ.
(13) ಆಕ್ಸ್ಲುಮೋ
ಕಂಪನಿ: ಅಲ್ನಿಲಾಮ್ ಫಾರ್ಮಾಸ್ಯುಟಿಕಲ್ಸ್ ಅಭಿವೃದ್ಧಿಪಡಿಸಿದೆ.
ಮಾರುಕಟ್ಟೆಗೆ ಸಮಯ: ನವೆಂಬರ್ 2020 ರಲ್ಲಿ ಮಾರ್ಕೆಟಿಂಗ್ಗಾಗಿ ಯುರೋಪಿಯನ್ ಒಕ್ಕೂಟದಿಂದ ಅನುಮೋದಿಸಲಾಗಿದೆ.
ಸೂಚನೆಗಳು: ಪ್ರಾಥಮಿಕ ಹೈಪರ್ಆಕ್ಸಲೂರಿಯಾ ಟೈಪ್ 1 (PH1) ಚಿಕಿತ್ಸೆಗಾಗಿ.
ಟೀಕೆಗಳು: Oxlumo ಹೈಡ್ರಾಕ್ಸಿಯಾಸಿಡ್ ಆಕ್ಸಿಡೇಸ್ 1 (HAO1) mRNA ಯನ್ನು ಗುರಿಯಾಗಿಸುವ siRNA ಔಷಧವಾಗಿದೆ, ಮತ್ತು ಆಡಳಿತ ವಿಧಾನವು ಸಬ್ಕ್ಯುಟೇನಿಯಸ್ ಇಂಜೆಕ್ಷನ್ ಆಗಿದೆ.ಅಲ್ನಿಲಾಮ್ನ ಇತ್ತೀಚಿನ ವರ್ಧಿತ ಸ್ಥಿರೀಕರಣ ರಸಾಯನಶಾಸ್ತ್ರ, ESC-GalNAc ಸಂಯೋಗ ತಂತ್ರಜ್ಞಾನವನ್ನು ಬಳಸಿಕೊಂಡು ಔಷಧವನ್ನು ಅಭಿವೃದ್ಧಿಪಡಿಸಲಾಗಿದೆ, ಇದು ಸಬ್ಕ್ಯುಟೇನಿಯಸ್ ಆಗಿ ನಿರ್ವಹಿಸಲಾದ siRNA ಯನ್ನು ಹೆಚ್ಚಿನ ನಿರಂತರತೆ ಮತ್ತು ಸಾಮರ್ಥ್ಯದೊಂದಿಗೆ ಸಕ್ರಿಯಗೊಳಿಸುತ್ತದೆ.ಔಷಧವು ಹೈಡ್ರಾಕ್ಸಿಯಾಸಿಡ್ ಆಕ್ಸಿಡೇಸ್ 1 (HAO1) mRNA ಯನ್ನು ಕುಗ್ಗಿಸುತ್ತದೆ ಅಥವಾ ಪ್ರತಿಬಂಧಿಸುತ್ತದೆ, ಯಕೃತ್ತಿನಲ್ಲಿ ಗ್ಲೈಕೊಲೇಟ್ ಆಕ್ಸಿಡೇಸ್ ಮಟ್ಟವನ್ನು ಕಡಿಮೆ ಮಾಡುತ್ತದೆ ಮತ್ತು ನಂತರ ಆಕ್ಸಲೇಟ್ ಉತ್ಪಾದನೆಗೆ ಅಗತ್ಯವಾದ ತಲಾಧಾರವನ್ನು ಸೇವಿಸುತ್ತದೆ, ರೋಗಿಗಳಲ್ಲಿ ರೋಗದ ಪ್ರಗತಿಯನ್ನು ನಿಯಂತ್ರಿಸಲು ಮತ್ತು ರೋಗದ ಲಕ್ಷಣಗಳನ್ನು ಸುಧಾರಿಸಲು ಆಕ್ಸಲೇಟ್ ಉತ್ಪಾದನೆಯನ್ನು ಕಡಿಮೆ ಮಾಡುತ್ತದೆ.
(14) ವಿಲ್ಟೆಪ್ಸೊ
ಕಂಪನಿ: ನಿಪ್ಪಾನ್ ಶಿನ್ಯಾಕುನ ಅಂಗಸಂಸ್ಥೆಯಾದ NS ಫಾರ್ಮಾದಿಂದ ಅಭಿವೃದ್ಧಿಪಡಿಸಲಾಗಿದೆ.
ಮಾರುಕಟ್ಟೆಗೆ ಸಮಯ: ಆಗಸ್ಟ್ 2020 ರಲ್ಲಿ ಮಾರ್ಕೆಟಿಂಗ್ಗಾಗಿ FDA ಯಿಂದ ಅನುಮೋದಿಸಲಾಗಿದೆ.
ಸೂಚನೆಗಳು: ಡಿಎಮ್ಡಿ ಜೀನ್ನಲ್ಲಿ ಎಕ್ಸಾನ್ 53 ಸ್ಕಿಪ್ಪಿಂಗ್ ಜೀನ್ ರೂಪಾಂತರದೊಂದಿಗೆ ಡುಚೆನ್ ಮಸ್ಕ್ಯುಲರ್ ಡಿಸ್ಟ್ರೋಫಿ (ಡಿಎಮ್ಡಿ) ಚಿಕಿತ್ಸೆಗಾಗಿ.
ಟೀಕೆಗಳು: ವಿಲ್ಟೆಪ್ಸೊ ಎನ್ನುವುದು ಆಂಟಿಸೆನ್ಸ್ ಆಲಿಗೊನ್ಯೂಕ್ಲಿಯೊಟೈಡ್ drug ಷಧವಾಗಿದ್ದು, ಇದು ಡಿಎಂಡಿ ಜೀನ್ನ ಪೂರ್ವ-ಎಂಆರ್ಎನ್ಎಯ ಎಕ್ಸಾನ್ 53 ರ ಸ್ಥಾನಕ್ಕೆ ಬಂಧಿಸಬಲ್ಲದು, ಇದರಿಂದಾಗಿ ಪ್ರಬುದ್ಧ ಎಮ್ಆರ್ಎನ್ಎ ರಚನೆಯ ನಂತರ ಎಕ್ಸಾನ್ 53 ರ ಭಾಗವನ್ನು ಹೊರಹಾಕಲು ಕಾರಣವಾಗುತ್ತದೆ, ಇದರಿಂದಾಗಿ ಎಮ್ಆರ್ಎನ್ಎ ಓದುವ ಚೌಕಟ್ಟನ್ನು ಭಾಗಶಃ ಸರಿಪಡಿಸುತ್ತದೆ ಪೆಟ್ಟಿಗೆಯನ್ನು ರೋಗಿಗಳಿಗೆ ಸಹಾಯ ಮಾಡುತ್ತದೆ.
(15) ಅಮಾಂಡಿಸ್ 45
ಕಂಪನಿ: ಸರೆಪ್ಟಾ ಥೆರಪ್ಯೂಟಿಕ್ಸ್ ಅಭಿವೃದ್ಧಿಪಡಿಸಿದೆ.
ಮಾರುಕಟ್ಟೆಗೆ ಸಮಯ: ಫೆಬ್ರವರಿ 2021 ರಲ್ಲಿ ಮಾರ್ಕೆಟಿಂಗ್ಗಾಗಿ FDA ಯಿಂದ ಅನುಮೋದಿಸಲಾಗಿದೆ.
ಸೂಚನೆಗಳು: ಡಿಎಮ್ಡಿ ಜೀನ್ನಲ್ಲಿ ಎಕ್ಸಾನ್ 45 ಸ್ಕಿಪ್ಪಿಂಗ್ ಜೀನ್ ರೂಪಾಂತರದೊಂದಿಗೆ ಡುಚೆನ್ ಮಸ್ಕ್ಯುಲರ್ ಡಿಸ್ಟ್ರೋಫಿ (ಡಿಎಮ್ಡಿ) ಚಿಕಿತ್ಸೆಗಾಗಿ.
ಟೀಕೆಗಳು: ಅಮೊಂಡಿಸ್ 45 ಒಂದು ಆಂಟಿಸೆನ್ಸ್ ಆಲಿಗೋನ್ಯೂಕ್ಲಿಯೊಟೈಡ್ ಔಷಧವಾಗಿದೆ, ಆಂಟಿಸೆನ್ಸ್ ಆಲಿಗೊನ್ಯೂಕ್ಲಿಯೊಟೈಡ್ ಡಿಎಮ್ಡಿ ಜೀನ್ನ ಪೂರ್ವ-ಎಂಆರ್ಎನ್ಎಯ ಎಕ್ಸಾನ್ 45 ರ ಸ್ಥಾನಕ್ಕೆ ಬಂಧಿಸುತ್ತದೆ, ಇದರ ಪರಿಣಾಮವಾಗಿ ಎಕ್ಸಾನ್ 45 ರ ಭಾಗವು ಪ್ರಬುದ್ಧ ಎಮ್ಆರ್ಎನ್ಎ ಎಕ್ಸೈಶನ್ ರಚನೆಯ ನಂತರ ನಿರ್ಬಂಧಿಸಲ್ಪಡುತ್ತದೆ, ತನ್ಮೂಲಕ ಎಮ್ಆರ್ಎನ್ಎ ಚೌಕಟ್ಟನ್ನು ಭಾಗಶಃ ಸಂಯೋಜಿಸಲು ಸಹಾಯ ಮಾಡುತ್ತದೆ. ಸಾಮಾನ್ಯ ಪ್ರೋಟೀನ್ಗಿಂತ ಚಿಕ್ಕದಾಗಿದೆ, ಇದರಿಂದಾಗಿ ರೋಗಿಯ ರೋಗಲಕ್ಷಣಗಳನ್ನು ಸುಧಾರಿಸುತ್ತದೆ.
(16) ಅಂವುತ್ರ (ವುಟ್ರಿಸಿರಾನ್)
ಕಂಪನಿ: ಅಲ್ನಿಲಾಮ್ ಫಾರ್ಮಾಸ್ಯುಟಿಕಲ್ಸ್ ಅಭಿವೃದ್ಧಿಪಡಿಸಿದೆ.
ಮಾರುಕಟ್ಟೆಗೆ ಸಮಯ: ಜೂನ್ 2022 ರಲ್ಲಿ ಮಾರ್ಕೆಟಿಂಗ್ಗಾಗಿ FDA ಯಿಂದ ಅನುಮೋದಿಸಲಾಗಿದೆ.
ಸೂಚನೆಗಳು: ವಯಸ್ಕರಲ್ಲಿ ಪಾಲಿನ್ಯೂರೋಪತಿ (hATTR-PN) ಜೊತೆಗೆ ಆನುವಂಶಿಕ ಟ್ರಾನ್ಸ್ಥೈರೆಟಿನ್ ಅಮಿಲೋಯ್ಡೋಸಿಸ್ ಚಿಕಿತ್ಸೆಗಾಗಿ.
ಟೀಕೆಗಳು: ಅಂವುತ್ರಾ (ವುಟ್ರಿಸಿರಾನ್) ಎಂಬುದು ಟ್ರಾನ್ಸ್ಥೈರೆಟಿನ್ (ಎಟಿಟಿಆರ್) ಎಮ್ಆರ್ಎನ್ಎ ಗುರಿಯಾಗಿಸುವ ಸಿಆರ್ಎನ್ಎ ಔಷಧವಾಗಿದ್ದು, ಸಬ್ಕ್ಯುಟೇನಿಯಸ್ ಇಂಜೆಕ್ಷನ್ ಮೂಲಕ ನಿರ್ವಹಿಸಲಾಗುತ್ತದೆ.Vutrisiran ಅಲ್ನಿಲಾಮ್ನ ವರ್ಧಿತ ಸ್ಥಿರತೆ ರಸಾಯನಶಾಸ್ತ್ರ (ESC)-GalNAc ಸಂಯೋಜಿತ ವಿತರಣಾ ವೇದಿಕೆಯ ವಿನ್ಯಾಸವನ್ನು ಹೆಚ್ಚಿದ ಸಾಮರ್ಥ್ಯ ಮತ್ತು ಚಯಾಪಚಯ ಸ್ಥಿರತೆಯನ್ನು ಆಧರಿಸಿದೆ.ಚಿಕಿತ್ಸೆಯ ಅನುಮೋದನೆಯು ಅದರ ಹಂತ III ಕ್ಲಿನಿಕಲ್ ಅಧ್ಯಯನದ (HELIOS-A) 9-ತಿಂಗಳ ಡೇಟಾವನ್ನು ಆಧರಿಸಿದೆ, ಮತ್ತು ಒಟ್ಟಾರೆ ಫಲಿತಾಂಶಗಳು ಚಿಕಿತ್ಸೆಯು hATTR-PN ನ ರೋಗಲಕ್ಷಣಗಳನ್ನು ಸುಧಾರಿಸಿದೆ ಎಂದು ತೋರಿಸುತ್ತದೆ ಮತ್ತು 50% ಕ್ಕಿಂತ ಹೆಚ್ಚು ರೋಗಿಗಳ ಸ್ಥಿತಿಯನ್ನು ಹಿಮ್ಮುಖಗೊಳಿಸಲಾಗಿದೆ ಅಥವಾ ಹದಗೆಡದಂತೆ ನಿಲ್ಲಿಸಲಾಗಿದೆ.
4. ಇತರ ಜೀನ್ ಥೆರಪಿ ಔಷಧಗಳು
(1) ರೆಕ್ಸಿನ್-ಜಿ
ಕಂಪನಿ: ಎಪಿಯಸ್ ಬಯೋಟೆಕ್ ಅಭಿವೃದ್ಧಿಪಡಿಸಿದೆ.
ಮಾರುಕಟ್ಟೆಗೆ ಸಮಯ: 2005 ರಲ್ಲಿ, ಫಿಲಿಪೈನ್ ಫುಡ್ ಅಂಡ್ ಡ್ರಗ್ ಅಡ್ಮಿನಿಸ್ಟ್ರೇಷನ್ (BFAD) ಮೂಲಕ ಇದನ್ನು ಮಾರ್ಕೆಟಿಂಗ್ ಮಾಡಲು ಅನುಮೋದಿಸಲಾಗಿದೆ.
ಸೂಚನೆಗಳು: ಕೀಮೋಥೆರಪಿಗೆ ನಿರೋಧಕವಾದ ಮುಂದುವರಿದ ಕ್ಯಾನ್ಸರ್ಗಳ ಚಿಕಿತ್ಸೆಗಾಗಿ.
ಟೀಕೆಗಳು: ರೆಕ್ಸಿನ್-ಜಿ ಜೀನ್-ಲೋಡ್ ನ್ಯಾನೊಪರ್ಟಿಕಲ್ ಇಂಜೆಕ್ಷನ್ ಆಗಿದೆ.ಇದು ನಿರ್ದಿಷ್ಟವಾಗಿ ಘನ ಗೆಡ್ಡೆಗಳನ್ನು ಕೊಲ್ಲಲು ರೆಟ್ರೊವೈರಲ್ ವೆಕ್ಟರ್ ಮೂಲಕ ಗುರಿಯ ಜೀವಕೋಶಗಳಿಗೆ ಸೈಕ್ಲಿನ್ G1 ರೂಪಾಂತರಿತ ಜೀನ್ ಅನ್ನು ಪರಿಚಯಿಸುತ್ತದೆ.ಆಡಳಿತದ ವಿಧಾನವು ಇಂಟ್ರಾವೆನಸ್ ಇನ್ಫ್ಯೂಷನ್ ಆಗಿದೆ.ಮೆಟಾಸ್ಟಾಟಿಕ್ ಕ್ಯಾನ್ಸರ್ ಕೋಶಗಳನ್ನು ಸಕ್ರಿಯವಾಗಿ ಹುಡುಕುವ ಮತ್ತು ನಾಶಪಡಿಸುವ ಗೆಡ್ಡೆ-ಉದ್ದೇಶಿತ ಔಷಧವಾಗಿ, ಉದ್ದೇಶಿತ ಜೈವಿಕ ಸೇರಿದಂತೆ ಇತರ ಕ್ಯಾನ್ಸರ್ ಔಷಧಗಳನ್ನು ವಿಫಲಗೊಳಿಸಿದ ರೋಗಿಗಳ ಮೇಲೆ ಇದು ಒಂದು ನಿರ್ದಿಷ್ಟ ಗುಣಪಡಿಸುವ ಪರಿಣಾಮವನ್ನು ಹೊಂದಿದೆ.
(2) ನಿಯೋವಾಸ್ಕಲ್ಜೆನ್
ಕಂಪನಿ: ಹ್ಯೂಮನ್ ಸ್ಟೆಮ್ ಸೆಲ್ ಇನ್ಸ್ಟಿಟ್ಯೂಟ್ನಿಂದ ಅಭಿವೃದ್ಧಿಪಡಿಸಲಾಗಿದೆ.
ಪಟ್ಟಿ ಮಾಡುವ ಸಮಯ: ಇದನ್ನು ಡಿಸೆಂಬರ್ 7, 2011 ರಂದು ರಷ್ಯಾದಲ್ಲಿ ಪಟ್ಟಿ ಮಾಡಲು ಅನುಮೋದಿಸಲಾಯಿತು ಮತ್ತು ನಂತರ 2013 ರಲ್ಲಿ ಉಕ್ರೇನ್ನಲ್ಲಿ ಪ್ರಾರಂಭಿಸಲಾಯಿತು.
ಸೂಚನೆಗಳು: ತೀವ್ರವಾದ ಅಂಗ ರಕ್ತಕೊರತೆಯ ಸೇರಿದಂತೆ ಬಾಹ್ಯ ನಾಳೀಯ ಅಪಧಮನಿಯ ಕಾಯಿಲೆಯ ಚಿಕಿತ್ಸೆಗಾಗಿ.
ಟೀಕೆಗಳು: ನಿಯೋವಾಸ್ಕಲ್ಜೆನ್ ಡಿಎನ್ಎ ಪ್ಲಾಸ್ಮಿಡ್ಗಳ ಆಧಾರದ ಮೇಲೆ ಜೀನ್ ಚಿಕಿತ್ಸೆಯಾಗಿದೆ.ನಾಳೀಯ ಎಂಡೋಥೀಲಿಯಲ್ ಬೆಳವಣಿಗೆಯ ಅಂಶ (VEGF) 165 ಜೀನ್ ಅನ್ನು ಪ್ಲಾಸ್ಮಿಡ್ ಬೆನ್ನೆಲುಬಿನ ಮೇಲೆ ನಿರ್ಮಿಸಲಾಗಿದೆ ಮತ್ತು ರೋಗಿಗಳಿಗೆ ತುಂಬಿಸಲಾಗುತ್ತದೆ.
(3) ಕೊಲಾಟೆಜೆನ್
ಕಂಪನಿ: ಒಸಾಕಾ ವಿಶ್ವವಿದ್ಯಾಲಯ ಮತ್ತು ಸಾಹಸೋದ್ಯಮ ಬಂಡವಾಳ ಕಂಪನಿಗಳಿಂದ ಜಂಟಿಯಾಗಿ ಅಭಿವೃದ್ಧಿಪಡಿಸಲಾಗಿದೆ.
ಮಾರುಕಟ್ಟೆಗೆ ಸಮಯ: ಆಗಸ್ಟ್ 2019 ರಲ್ಲಿ ಜಪಾನ್ನ ಆರೋಗ್ಯ, ಕಾರ್ಮಿಕ ಮತ್ತು ಕಲ್ಯಾಣ ಸಚಿವಾಲಯವು ಅನುಮೋದಿಸಿದೆ.
ಸೂಚನೆಗಳು: ನಿರ್ಣಾಯಕ ಕೆಳ ತುದಿಗಳ ರಕ್ತಕೊರತೆಯ ಚಿಕಿತ್ಸೆ.
ಟೀಕೆಗಳು: Collategene ಒಂದು ಪ್ಲಾಸ್ಮಿಡ್-ಆಧಾರಿತ ಜೀನ್ ಚಿಕಿತ್ಸೆಯಾಗಿದೆ, ಇದು ಜಪಾನಿನ ಜೀನ್ ಥೆರಪಿ ಕಂಪನಿಯಾದ AnGes ನಿಂದ ಉತ್ಪಾದಿಸಲ್ಪಟ್ಟ ಮೊದಲ ದೇಶೀಯ ಜೀನ್ ಚಿಕಿತ್ಸೆ ಔಷಧವಾಗಿದೆ.ಈ ಔಷಧದ ಮುಖ್ಯ ಅಂಶವೆಂದರೆ ಮಾನವ ಹೆಪಟೊಸೈಟ್ ಬೆಳವಣಿಗೆಯ ಅಂಶ (HGF) ಜೀನ್ ಅನುಕ್ರಮವನ್ನು ಹೊಂದಿರುವ ನೇಕೆಡ್ ಪ್ಲಾಸ್ಮಿಡ್.ಕೆಳಗಿನ ಅಂಗಗಳ ಸ್ನಾಯುಗಳಿಗೆ ಔಷಧವನ್ನು ಚುಚ್ಚಿದರೆ, ವ್ಯಕ್ತಪಡಿಸಿದ HGF ಮುಚ್ಚಿದ ರಕ್ತನಾಳಗಳ ಸುತ್ತಲೂ ಹೊಸ ರಕ್ತನಾಳಗಳ ರಚನೆಯನ್ನು ಉತ್ತೇಜಿಸುತ್ತದೆ.ಕ್ಲಿನಿಕಲ್ ಪ್ರಯೋಗಗಳು ಹುಣ್ಣುಗಳನ್ನು ಸುಧಾರಿಸುವಲ್ಲಿ ಅದರ ಪರಿಣಾಮವನ್ನು ದೃಢಪಡಿಸಿವೆ.
ಜೀನ್ ಥೆರಪಿ ಅಭಿವೃದ್ಧಿಗೆ ಫೋರ್ಜೀನ್ ಹೇಗೆ ಸಹಾಯ ಮಾಡುತ್ತದೆ?
siRNA ಔಷಧ ಅಭಿವೃದ್ಧಿಯ ಆರಂಭಿಕ ಹಂತದಲ್ಲಿ ದೊಡ್ಡ ಪ್ರಮಾಣದ ಸ್ಕ್ರೀನಿಂಗ್ನಲ್ಲಿ ಸ್ಕ್ರೀನಿಂಗ್ ಸಮಯವನ್ನು ಉಳಿಸಲು ನಾವು ಸಹಾಯ ಮಾಡುತ್ತೇವೆ.
ಹೆಚ್ಚಿನ ವಿವರಗಳಿಗೆ ಭೇಟಿ ನೀಡಿ:
https://www.foreivd.com/cell-direct-rt-qpcr-kit-direct-rt-qpcr-series/
ಪೋಸ್ಟ್ ಸಮಯ: ಡಿಸೆಂಬರ್-27-2022